题目内容
12.用试管分别取的等量5%的H2O2溶液进行实验,下列分解速率最快的条件组合是( )①40℃热水中 ②5℃冷水中 ③加入FeCl3 ④不加催化剂.
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ②③ |
分析 根据温度越高,加催化剂将加大化学反应速率来分析.
解答 解:温度越高,反应速率越快,使用催化剂加快反应,所以①③分解速率最快.
故选:B.
点评 此题考查了影响反应速率快慢的因素,比较容易,一般来说,温度对化学反应速率的影响要比浓度、压强的影响大.

练习册系列答案
相关题目
2.在一定温度下,硫酸铜晶体的培养皿中存在下列平衡:Cu2++SO42-+x H2O?CuSO4•xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是( )
| A. | 溶液中Cu2+浓度增大 | B. | 溶液中Cu2+数目减少 | ||
| C. | 该硫酸铜晶体体积增大 | D. | 溶液的蓝色变浅 |
17.燃料电池是一种高效、环境友好的发电装置.以H2为燃料时,产物为H2O;以CH4为燃料时,产物为H2O和CO2.下列说法不正确的是( )
| A. | H2、CH4在负极失去电子,发生氧化反应 | |
| B. | 从产物推断,两种燃料电池的氧化剂均为O2 | |
| C. | 燃料电池将化学能直接转变为电能,能量转化率高 | |
| D. | 分别将1 mol H2与1 mol CH4做燃料电池的燃料,转移的电子一样多 |
1.关于合成氨反应N2(g)+3H2(g)?2NH3(g)达到限度时,下列叙述正确的是( )
| A. | N2和H2全部转化为NH3 | |
| B. | 正反应和逆反应的化学反应速率均为零 | |
| C. | N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| D. | 若外界条件发生改变,化学反应的限度可能随之改变 |
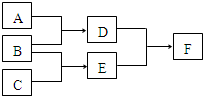 单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:
单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:


