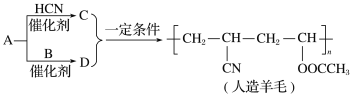
题目内容
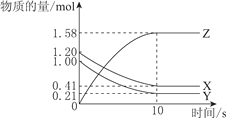
【题目】下图表示取1 mol己烯雌酚进行的四个实验,下列对实验数据的预测与实际情况吻合的是
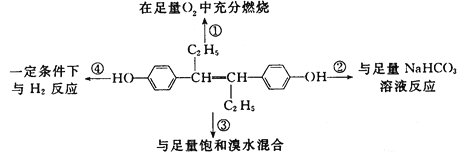
A. ①中生成7 mol H2O B. ②中生成2 mol CO2
C. ③中最多消耗3 mo1 Br2 D. ④中最多消耗7 mol H2
【答案】D
【解析】试题分析:A、由己烯雌酚的结构简式知,1mol己烯雌酚中含22mol氢原子,由氢原子守恒可知,①中生成11mol H2O,错误;B、由己烯雌酚的结构简式知,己烯雌酚的官能团为碳碳双键和酚羟基,与碳酸氢钠溶液不反应,则②中无CO2生成,错误;C、由己烯雌酚的结构简式知,1mol己烯雌酚中含有1mol碳碳双键,可与1mol Br2发生加成反应;1mol己烯雌酚中含有2mol酚羟基,酚羟基邻、对位上的氢原子均可与溴发生取代反应,取代1molH用1mol Br2,1mol己烯雌酚中共有4 mol邻、对位H原子可被取代,则③中最多消耗5mol Br2,错误;D、苯环与碳碳双键都能与氢气发生加成反应,1mol己烯雌酚与氢气发生加成反应,最多消耗7mol氢气,正确。

【题目】如表列出了①~⑥六种元素在元素周期表中的位置.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是 (填写元素符号);
(2)元素①③⑥的氢化物的分子式分别是 ; ; .
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是 .
【题目】(12分)下表为长式周期表的一部分,其中的编号代表对应的元素。
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | [ | ⑦ | |||||||||||||
⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区元素的是 (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为________________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑦和⑧形成的化合物的电子式为 。
(6)元素⑩的基态原子核外电子排布式是 。
(7)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
_______________________________________________。