题目内容
【题目】核电荷数 1~18 的四种元素 W、X、Y、Z,原子序数依次变小,原子核外电子层数之和是 8。W 单质是银白色固体、导电性强,在空气中燃烧发出黄色的火焰;X 元素原子最外层电子层上的电子数 是 Y 和 Z 两元素原子最外层上的电子数的总和;Y 元素原子的最外电子层上的电子数是它的电子层数 的 2 倍,X 和 Z 可以形成 XZ3 的化合物,请回答:
(1)X 元素的原子结构示意图是________________;Y 元素的名称是________________;Z 的阴 离子的电子式:________________。
(2)分别写出 X、Y 的最高价含氧酸的化学式________________、________________。
(3)W 和 X 可形成化合物,它能与水剧烈反应产生 XZ3,所发生的化学方程式为:________________,该化合物中 W 离子的电子式为________________。
【答案】 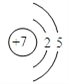 碳 [H :] HNO3 H2CO3 Na3N+3H2O→NH3↑+3NaOH Na+
碳 [H :] HNO3 H2CO3 Na3N+3H2O→NH3↑+3NaOH Na+
【解析】W 单质是银白色固体、导电性强,在空气中燃烧发出黄色的火焰,可知W为Na元素;四元素原子核外电子层数之和是8,则Z处于第一周期,X和Y处于第二周期,可推知Z为H元素;Y 元素原子的最外电子层上的电子数是它的电子层数 的 2 倍,则Y为碳元素,X 元素原子最外层电子层上的电子数 是 Y 和 Z 两元素原子最外层上的电子数的总和,则X元素的最外层电子数为5,为氮元素;
(1)X 为氮元素,核电荷数为7,其原子结构示意图是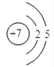 ;Y 元素的名称是碳;氢的阴 离子的电子式为[H :];
;Y 元素的名称是碳;氢的阴 离子的电子式为[H :];
(2)N的最高价为+5价、C的最高价为+4价,它们对应的最高价含氧酸的化学式为HNO3、H2CO3;
(3)Na和N 可形成离子化合物Na3N,它能与水剧烈反应产生 NH3,所发生的化学方程式为Na3N+3H2O=NH3↑+3NaOH,离子化合物Na3N中 钠离子的电子式为Na+。