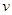题目内容
已知反应 2NH3 N2 + 3H2,在某温度下的平衡常数为0.25,那么,在此条件下,氨的合成反应1/2 N2 + 3/2 H2
N2 + 3H2,在某温度下的平衡常数为0.25,那么,在此条件下,氨的合成反应1/2 N2 + 3/2 H2 NH3的平衡常数为
NH3的平衡常数为
 N2 + 3H2,在某温度下的平衡常数为0.25,那么,在此条件下,氨的合成反应1/2 N2 + 3/2 H2
N2 + 3H2,在某温度下的平衡常数为0.25,那么,在此条件下,氨的合成反应1/2 N2 + 3/2 H2 NH3的平衡常数为
NH3的平衡常数为| A.4 | B.2 | C.1 | D.0.5 |
B
逆反应的平衡常数就是正反应的平衡常数的倒数,所以该反应的平衡常数是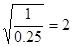 ,答案选B。
,答案选B。
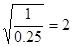 ,答案选B。
,答案选B。
练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
 2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( ) Na2S(s)+4H2O(g)
Na2S(s)+4H2O(g)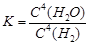
 N2O4在恒容容器中进行,当体系压强不再发生变化时,反应达到化学平衡状态
N2O4在恒容容器中进行,当体系压强不再发生变化时,反应达到化学平衡状态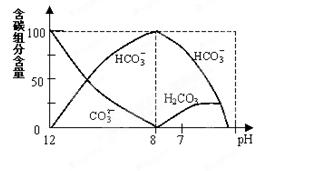
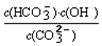 =2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
=2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。 CH3OH(g) ΔH1
CH3OH(g) ΔH1 a、容器各物质的浓度保持不变; b、容器内压强保持不变;
a、容器各物质的浓度保持不变; b、容器内压强保持不变;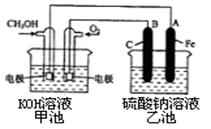
 2C(g),5min后各容器反应达平衡状态,其中甲容器中A的物质的量为0.4mol。
2C(g),5min后各容器反应达平衡状态,其中甲容器中A的物质的量为0.4mol。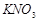 的溶解度s
的溶解度s