题目内容
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、Na+、Cu2+、Cl-、NO3- |
| B、Na+、NO3-、H+、CO32- |
| C、MnO4-、K+、HCO3- |
| D、K+、Na+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:碱性溶液中,含大量的OH-,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,并结合离子的颜色来解答.
解答:
解:A.Cu2+、OH结合生成沉淀,不能共存,且Cu2+为蓝色,与无色不符,故A不选;
B.H+、CO32-结合生成水和气体,H+、OH-结合生成水,不能共存,故B不选;
C.OH-、HCO32-结合生成水和碳酸根离子,不能共存,且MnO4-为紫色,与无色不符,故C不选;
D.该组离子之间不反应,可大量共存,且离子均为无色,故D选;
故选D.
B.H+、CO32-结合生成水和气体,H+、OH-结合生成水,不能共存,故B不选;
C.OH-、HCO32-结合生成水和碳酸根离子,不能共存,且MnO4-为紫色,与无色不符,故C不选;
D.该组离子之间不反应,可大量共存,且离子均为无色,故D选;
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意常见离子的颜色,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、22.4L O2中含有NA个氧分子 |
| B、2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
| C、18g H2O所含电子数目为10NA |
| D、在25℃,压强为1.01×105Pa时,11.2L氮气所含的原子数目为NA |
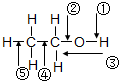 乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )
乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )| A、和金属钠反应时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、乙醇完全燃烧时,断裂键①② |
| D、在铜催化下和氧气反应时,键①和③断裂 |
将Li3N固体溶于水中,产生了大量的氨气,下列有关此过程中的说法,正确的是( )
| A、产生氨气过程无能量变化 |
| B、Li3N中只含有离子键 |
| C、Li3N中含有离子键、共价键 |
| D、产生氨气过程有电子转移 |
下列说法不正确的说法是( )
| A、阿司匹林具有解热镇痛作用 |
| B、长期饮用纯净水,有可能引起一些微量元素缺乏症 |
| C、Al(OH)3能用于治疗胃酸过多 |
| D、使用青霉素时,直接静脉注射可以不用进行皮肤敏感测试 |
与反应Cl2+SO2+2H2O=H2SO4+2HCl中水的作用完全相同的是( )
A、2H2O
| ||||
| B、Cl2+H2O=HCl+HClO | ||||
C、3Fe+4H2O(g)
| ||||
| D、2Na+2H2O=2NaOH+H2↑ |