题目内容
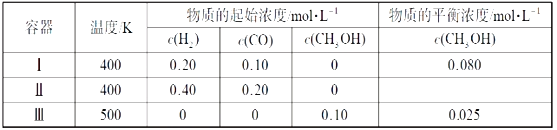
【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g)达到平衡。下列说法正确的是( )
CH3OH(g)达到平衡。下列说法正确的是( )
A.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
B.该反应的正反应放热
C.达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小
【答案】B
【解析】
A.容器Ⅱ装入的量是容器Ⅰ的两倍,可以先理解为2个容器Ⅰ,每个容器都装的和容器Ⅰ的量一样,平衡时两者的转化率相等,再将容器Ⅱ压缩到只有一个容器Ⅰ大小,加压,平衡向物质的量减小的反应方向即正向移动,反应物又消耗,因此达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小,故A错误;
B.分析Ⅰ、Ⅲ中数据知反应开始时Ⅰ中加入的H2、CO与Ⅲ中加入甲醇的物质的量相当,平衡时甲醇的浓度:Ⅰ>Ⅲ,温度:Ⅰ<Ⅲ,即升高温度平衡逆向移动,逆向为吸热反应,正向为放热反应,故B正确;
C.根据A选项分析得出容器Ⅱ中c(H2)小于容器Ⅰ中c(H2)的两倍,根据B选项分析得出容器Ⅲ中c(H2)比容器Ⅰ中c(H2)大,因此容器Ⅱ中c(H2)小于容器Ⅲ中c(H2)的两倍,故C错误;
D.温度:Ⅲ>Ⅰ,当其他条件不变时,升高温度反应速率加快,故达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大,故D错误。
综上所述,答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目