题目内容
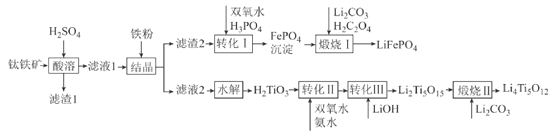
【题目】以废旧锂离子电池的正极材料(主要含LiCoO2、Al、C等)为原料制备CoC2O4.2H2O的一种实验流程如图:
![]()
![]()
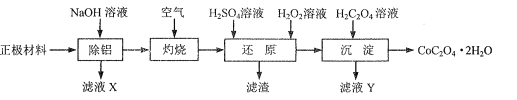
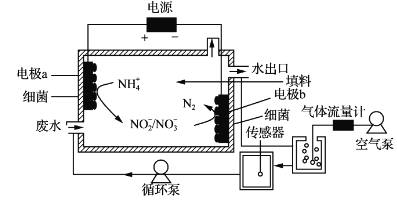
(1)“除铝”可在如图1所示的装置中进行。保持温度、反应物和溶剂的量不变,实验中提高铝的去除率的措施有___。
(2)“灼烧”的主要目的是___。
(3)“还原”步骤温度在70℃左右,LiCoO2发生反应的化学方程式为___。若该步骤用盐酸代替H2SO4和H2O2,也可达到“还原”的目的,但其缺点是___。
(4)“沉淀”步骤中,证明Co2+已沉淀完全的实验操作及现象是___。
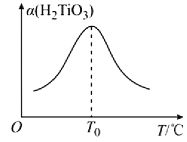
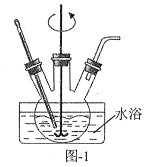
(5)设计由“滤液X”制备纯净的Al2O3的实验方案。(已知含铝物种浓度与pH的关系如图所示。实验中必须使用的试剂:H2SO4溶液、BaCl2溶液、蒸馏水)___。
【答案】加快反应速率或延长反应时间 除去C 2LiCoO2+3H2SO4+H2O2![]() 2CoSO4+Li2SO4+O2+4H2O 会产生有毒的Cl2 静置,在上层清液中继续滴加H2C2O4溶液,若不出现浑浊,则Co2+已沉淀完全 向“滤液X”中滴加H2SO4溶液,适时用pH试纸测溶液的pH,当pH介于6~8时,过滤,用蒸馏水洗涤沉淀,直至滤液加BaCl2溶液不再出现白色浑浊为止,将所得沉淀灼烧至沉淀不再减少,冷却,即得Al2O3
2CoSO4+Li2SO4+O2+4H2O 会产生有毒的Cl2 静置,在上层清液中继续滴加H2C2O4溶液,若不出现浑浊,则Co2+已沉淀完全 向“滤液X”中滴加H2SO4溶液,适时用pH试纸测溶液的pH,当pH介于6~8时,过滤,用蒸馏水洗涤沉淀,直至滤液加BaCl2溶液不再出现白色浑浊为止,将所得沉淀灼烧至沉淀不再减少,冷却,即得Al2O3
【解析】
正极材料主要含LiCoO2、Al、C,加入NaOH溶液,Al与NaOH反应生成NaAlO2溶液,剩余固体在空气中灼烧,C变成CO2,剩余的LiCoO2与H2SO4溶液和H2O2溶液发生氧化还原反应:2LiCoO2+3H2SO4+H2O2![]() 2CoSO4+Li2SO4+O2+4H2O,沉淀时发生反应Co2++C2O42-+2H2O===CoC2O4·2H2O,得到滤液Y为LiSO4等,根据分析可以解答问题。
2CoSO4+Li2SO4+O2+4H2O,沉淀时发生反应Co2++C2O42-+2H2O===CoC2O4·2H2O,得到滤液Y为LiSO4等,根据分析可以解答问题。
根据上述分析可得:
(1) 提高铝的去除率的措施有加快反应速率或延长反应时间,故答案为:加快反应速率或延长反应时间;
(2) 剩余固体在空气中灼烧,C变成CO2,因此灼烧的目的是除去C,故答案为除去C;
(3) LiCoO2与H2SO4溶液和H2O2溶液发生氧化还原反应,反应方程式为:2LiCoO2+3H2SO4+H2O2![]() 2CoSO4+Li2SO4+O2+4H2O,故答案为:2LiCoO2+3H2SO4+H2O2
2CoSO4+Li2SO4+O2+4H2O,故答案为:2LiCoO2+3H2SO4+H2O2![]() 2CoSO4+Li2SO4+O2+4H2O;
2CoSO4+Li2SO4+O2+4H2O;
(4) 用盐酸代替H2SO4和H2O2,也可达到“还原”的目的,但会产生有毒的Cl2,故答案为:会产生有毒的Cl2;
(5)证明Co2+已沉淀完全的实验操作及现象:静置,在上层清液中继续滴加H2C2O4溶液,若不出现浑浊,则Co2+已沉淀完全;
(6) “滤液X”为NaAlO2溶液,由“滤液X”制备纯净的Al2O3的实验方案为:向“滤液X”中滴加H2SO4溶液,适时用pH试纸测溶液的pH,当pH介于6~8时,过滤,用蒸馏水洗涤沉淀,直至滤液加BaCl2溶液不再出现白色浑浊为止,将所得沉淀灼烧至沉淀不再减少,冷却,即得Al2O3。

 名校课堂系列答案
名校课堂系列答案