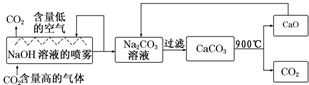
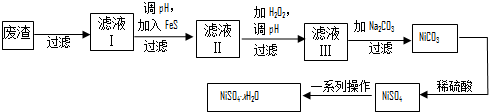
题目内容
16.下列制取氢气的方法中,反应速率最小的是( )| A. | 10℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| B. | 50℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| C. | 10℃时,块状锌与3 mol/L硫酸溶液反应 | |
| D. | 50℃时,块状锌与3 mol/L硫酸溶液反应 |
分析 题中涉及影响反应速率的因素有温度、固体的表面积大小,一般来说,温度越高,固体的表面积越大,则反应速率越大,反之越小,以此解答.
解答 解:B、D选项中温度较高,速率大于A、C,A、C的浓度相同,但A为粉末状固体,表面较大,反应速率较大,则反应速率最小的为C,
故选C.
点评 本题考查化学反应速率的影响因素,侧重于学生的分析能力的考查,为高考高频考点,注意把握影响反应速率的因素,注重相关知识的学习与积累,难度不大.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
4.对于可逆反应:2A(g)+2B(g)?3C(g)+D(s),减少压强产生的影响的是( )
| A. | 正反应速率加快,逆反应速率减慢,平衡向正反应方向移动 | |
| B. | 逆反应速率加快,正反应速率减慢,平衡向逆反应方向移动 | |
| C. | 正、逆反应速率都不变,平衡向逆反应方向移动 | |
| D. | 正、逆反应速率都减慢,平衡向逆反应方向移动 |
11.某溶液中可能含有SO42-、CO32-等.为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( )
| A. | H2SO4溶液 | B. | HCl溶液 | C. | NaOH溶液 | D. | NaNO3溶液 |
1.下列有关说法正确的是( )
| A. | 漂白粉久置于空气中会增加漂白效果 | |
| B. | 以海水为原料能制取Na、HCl、Mg、Br2等物质 | |
| C. | 蓝铜矿[Cu3(OH)2(CO3)2]也可表示为3CuO•2CO2•2H2O | |
| D. | 二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
8.对于反应中的能量变化,下列表述正确的是( )
| A. | 断开化学键的过程会放出能量 | |
| B. | 氧化反应均为吸热反应 | |
| C. | 加热才能发生的反应一定是吸热反应 | |
| D. | 放热反应中,反应物的总能量大于生成物的总能量 |
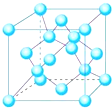 有X、Y、Z、W、P、Q六种前两周期的主族元素,原子序数依次增大,价电子数之和为26,原子半径依Y、Z、W、P、Q、X依次减小.围绕上述元素,回答下列问题:
有X、Y、Z、W、P、Q六种前两周期的主族元素,原子序数依次增大,价电子数之和为26,原子半径依Y、Z、W、P、Q、X依次减小.围绕上述元素,回答下列问题: ,YQ3中心原子的杂化类型为sp2杂化,除X外,其余元素的第一电离能由小到大顺序为B<C<O<N<F(元素符号回答).
,YQ3中心原子的杂化类型为sp2杂化,除X外,其余元素的第一电离能由小到大顺序为B<C<O<N<F(元素符号回答).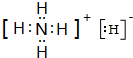 ,其与水反应的化学方程式为NH4H+H2O=NH3•H2O+H2↑.
,其与水反应的化学方程式为NH4H+H2O=NH3•H2O+H2↑.
 ;该微粒的表示符号为O2-.
;该微粒的表示符号为O2-.