题目内容
7.硅橡胶 是由
是由 经两种反应而制得的,这两种反应依次是( )
经两种反应而制得的,这两种反应依次是( )| A. | 消去、加聚 | B. | 水解、缩聚 | C. | 氧化、缩聚 | D. | 取代、加聚 |
分析 由二甲基二氯硅烷制得硅橡胶的反应流程为 ,有机物中卤素原子被羟基代替的反应,属于卤代烃的水解反应,含有两个羟基的有机物分子内脱去水会得到高分子化合物,以此解答该题.
,有机物中卤素原子被羟基代替的反应,属于卤代烃的水解反应,含有两个羟基的有机物分子内脱去水会得到高分子化合物,以此解答该题.
解答 解:硅橡胶是由二甲基二氯硅烷经过两种类型的反应而形成的高分子化合物: ,
,
在 中,前一步实现了有机物中卤素原子被羟基代替的反应,属于卤代烃的水解反应,然后是两分子的羟基脱去水分子形成了高聚物,属于缩聚反应,
中,前一步实现了有机物中卤素原子被羟基代替的反应,属于卤代烃的水解反应,然后是两分子的羟基脱去水分子形成了高聚物,属于缩聚反应,
故选B.
点评 本题考查了聚合反应原理、有机反应类型的判断,为高频考点,题目难度不大,注意掌握常见有机反应类型、反应原理,能够根据高分子化合物的结构判断其单体.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
18.下列说法不正确的是( )
| A. | 同族元素,随着电子层的增加,I1逐渐增大 | |
| B. | 通常情况下,电离能I1<I2<I3 | |
| C. | 同周期元素,随着核电荷数的增加,I1呈增大趋势 | |
| D. | 电离能越小,元素的金属性越强 |
15.用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰来制备A12(SO4)3.18H2O.,工艺流程如下(部分操作和条件略):
Ⅰ、向铝灰中加入过量稀H2SO4,过滤:
Ⅱ、向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ、加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ、加入MnSO4至紫红色消失,过滤;
Ⅴ、浓缩、结晶、分离,得到产品.
(1)铝在元素周期表中的位置第三周期ⅢA族;H2SO4溶解Al2O3的离子方程式是:Al2O3+6H+=2Al3++3H2O.
(2)写出Ⅱ中加入过量KMnO4溶液发生的离子方程式:5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O.
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:将Fe2+氧化为Fe3+,调节pH值使铁元素完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(5)在该实验条件下Ksp[Fe(OH)3]=4.0×10-38,当溶液的pH=3时,溶液中c(Fe3+)=4.0×10-5 mol/L.
Ⅰ、向铝灰中加入过量稀H2SO4,过滤:
Ⅱ、向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ、加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ、加入MnSO4至紫红色消失,过滤;
Ⅴ、浓缩、结晶、分离,得到产品.
(1)铝在元素周期表中的位置第三周期ⅢA族;H2SO4溶解Al2O3的离子方程式是:Al2O3+6H+=2Al3++3H2O.
(2)写出Ⅱ中加入过量KMnO4溶液发生的离子方程式:5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O.
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:将Fe2+氧化为Fe3+,调节pH值使铁元素完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(5)在该实验条件下Ksp[Fe(OH)3]=4.0×10-38,当溶液的pH=3时,溶液中c(Fe3+)=4.0×10-5 mol/L.
2. 白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )
 白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )| A. | (6a+5d-4c-12b) kJ | B. | (4c+12b-6a-5d) kJ | C. | (4c+12b-4a-5d) kJ | D. | (5a+5d-4c-12b) kJ |
12. 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )| A. | 三种元素的原子半径的大小顺序是B<A<C | |
| B. | A元素最高价氧化物对应水化物具有强氧化性和不稳定性 | |
| C. | B元素的氧化物和氢化物的水溶液都呈酸性 | |
| D. | C元素的单质是非金属单质中唯一能跟水激烈反应的单质 |

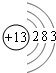 ,它的单质能(填能或不能)与氢氧化钠溶液反应.
,它的单质能(填能或不能)与氢氧化钠溶液反应.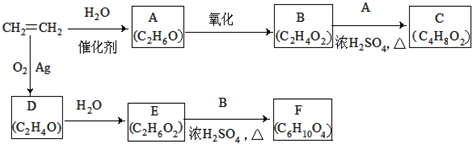
 .
. .
.