题目内容
在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是( )
| A、在c(H+)=10-10mol/L的溶液中:Al3+、NH4+、Cl-、NO3- |
| B、pH=13的溶液中:K+、Na+、SO32-、Cl- |
| C、pH=2的溶液中:K+、NH4+、Cl-、ClO- |
| D、甲基橙呈红色的溶液中:Fe3+、Na+、SO42-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:A.在c(H+)=10-10mol/L的溶液为碱性溶液,铝离子、铵根离子能够与氢氧根离子反应;
B.pH=13的溶液中存在存在大量的氢氧根离子,K+、Na+、SO32-、Cl-之间不发生反应,也不与氢氧根离子反应;
C.pH=2的溶液为酸性溶液,次氯酸根离子能够与氢离子反应生成次氯酸;
D.甲基橙呈红色的溶液为酸性溶液,铁离子与碳酸根离子发生双水解反应,碳酸根离子能够与氢离子反应.
B.pH=13的溶液中存在存在大量的氢氧根离子,K+、Na+、SO32-、Cl-之间不发生反应,也不与氢氧根离子反应;
C.pH=2的溶液为酸性溶液,次氯酸根离子能够与氢离子反应生成次氯酸;
D.甲基橙呈红色的溶液为酸性溶液,铁离子与碳酸根离子发生双水解反应,碳酸根离子能够与氢离子反应.
解答:
解:A.c(H+)=10-10mol/L的溶液中,氢氧根离子浓度为0.01mol/L,Al3+、NH4+能够与OH-离子反应,在溶液中不能大量共存,故A错误;
B.pH=13的溶液为碱性溶液,K+、Na+、SO32-、Cl-之间不反应,且都不与碱溶液反应,在溶液中能够大量共存,故B正确;
C.pH=2的溶液中存在大量的H+,ClO-能够与H+反应生成弱电解质次氯酸,在溶液中不能大量共存,故C错误;
D.甲基橙呈红色的溶液中存在大量氢离子,CO32-能够与Fe3+、H+发生反应,在溶液中不能大量共存,故D错误;
故选B.
B.pH=13的溶液为碱性溶液,K+、Na+、SO32-、Cl-之间不反应,且都不与碱溶液反应,在溶液中能够大量共存,故B正确;
C.pH=2的溶液中存在大量的H+,ClO-能够与H+反应生成弱电解质次氯酸,在溶液中不能大量共存,故C错误;
D.甲基橙呈红色的溶液中存在大量氢离子,CO32-能够与Fe3+、H+发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-等.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | ||||
B、苯酚钠溶液中通入少量的CO2:2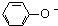 +CO2+H2O→ +CO2+H2O→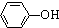 +CO32- +CO32- | ||||
C、用铜做电极电解CuSO4溶液:2Cu2++2H2O
| ||||
D、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-
|
下列排列顺序正确的是( )
| A、热稳定性强弱:HCl>HBr>HI |
| B、微粒半径:Cl->K+>Na+>Fe(OH)3胶粒 |
| C、晶体熔点:SiO2>NaCl>CF4>CCl4 |
| D、氢化物的沸点:H2Se>H2S>H2O |
下列物质中,S元素的化合价为+6的是( )
| A、S |
| B、H2SO4 |
| C、SO2 |
| D、H2S |
下列反应中,属于取代反应的是( )
| A、乙醇在一定条件下与氧气反应生成乙醛 |
| B、苯的硝化反应 |
| C、乙烯在一定条件下生成聚乙烯 |
| D、乙烯与溴的四氯化碳溶液反应 |
下列说法中正确的是( )
| A、碘和四氯化碳可以用分液漏斗进行分离 |
| B、将O2和H2的混合气体通过灼热的氧化铜,可以除去其中的氢气 |
| C、熔融烧碱时,可以使用铁坩埚 |
| D、加热铝箔,待铝熔化后,可以看到液态铝滴落下来 |
NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B、由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C、标准状况下,22.4L H2O中含氢原子数为2NA |
| D、制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |
下列各组分子中,都属于含有极性键的非极性分子的一组是( )
| A、CO2、H2O |
| B、C2H4、CH4 |
| C、Cl2、C2H2 |
| D、NH3、HCl |
下列化学用语表述正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、水分子的电子式: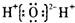 |
C、甲烷分子的比例模型: |
D、氯离子的结构示意图: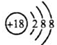 |