题目内容
下列化学用语表述正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、水分子的电子式: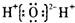 |
C、甲烷分子的比例模型: |
D、氯离子的结构示意图: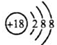 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.乙烯的结构简式必须标出官能团碳碳双键;
B.水分子为共价化合物,分子中不存在阴阳离子;
C.甲烷为正四面体结构,分子中存在4个碳氢键,碳原子半径大于氢原子;
D.氯离子的核电荷数为17,核外电子总数为18,最外层为8个电子.
B.水分子为共价化合物,分子中不存在阴阳离子;
C.甲烷为正四面体结构,分子中存在4个碳氢键,碳原子半径大于氢原子;
D.氯离子的核电荷数为17,核外电子总数为18,最外层为8个电子.
解答:
解:A.乙烯的官能团为碳碳双键,结构简式中必须标出官能团,乙烯正确的结构简式为:CH2=CH2,故A错误;
B.水分子不属于离子化合物,电子式中不能标出电荷,水的电子式为: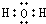 ,故B错误;
,故B错误;
C.甲烷分子中存在4个碳氢键,为正四面体结构,碳原子半径大于氢原子,甲烷分子的比例模型为: ,故C正确;
,故C正确;
D.氯离子的核电荷数为17,最外层为8个电子,氯离子正确的电子式为: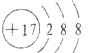 ,故D错误;
,故D错误;
故选C.
B.水分子不属于离子化合物,电子式中不能标出电荷,水的电子式为:
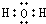 ,故B错误;
,故B错误;C.甲烷分子中存在4个碳氢键,为正四面体结构,碳原子半径大于氢原子,甲烷分子的比例模型为:
 ,故C正确;
,故C正确;D.氯离子的核电荷数为17,最外层为8个电子,氯离子正确的电子式为:
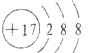 ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式、比例模型、离子结构示意图、结构简式的判断,题目难度不大,注意掌握掌握化学用语的概念及正确的表示方法,明确离子结构示意图与原子结构示意图的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是( )
| A、在c(H+)=10-10mol/L的溶液中:Al3+、NH4+、Cl-、NO3- |
| B、pH=13的溶液中:K+、Na+、SO32-、Cl- |
| C、pH=2的溶液中:K+、NH4+、Cl-、ClO- |
| D、甲基橙呈红色的溶液中:Fe3+、Na+、SO42-、CO32- |
下列过程或应用不涉及氧化还原反应的是( )
| A、工业上以Cl2和Ca(OH)2为原料制备漂白粉 |
| B、FeCl3溶液“腐蚀”Cu板 |
| C、Na2O2用作呼吸面具的供氧剂 |
| D、利用Al2(SO4)3和氨水反应来制取氢氧化铝 |
下列有关化学用语表述正确的是( )
A、CO2的电子式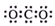 | ||
B、Cl-的结构示意图 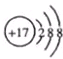 | ||
| C、次氯酸的结构式 H-Cl-O | ||
D、质量数为37的氯原子
|
下列各项中表达正确的是( )
A、F-的结构示意图: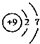 |
B、CO2的分子模型示意图: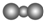 |
C、CSO的电子式: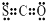 |
| D、N2的结构式:N≡N: |
CO2通入下列各溶液中,不能产生沉淀的是( )
| A、CaCl2溶液 |
| B、Na2SiO3溶液 |
| C、Ca(OH)2溶液 |
| D、Ba(OH)2溶液 |
甲、乙两种金属性质比较:
①甲的单质熔、沸点比乙的低;
②常温下,甲能与水反应放出氢气而乙不能;
③最高价氧化物对应的水化物碱性比较,乙比甲的强;
④甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡.
上述项目中能够说明甲比乙的金属性强的是( )
①甲的单质熔、沸点比乙的低;
②常温下,甲能与水反应放出氢气而乙不能;
③最高价氧化物对应的水化物碱性比较,乙比甲的强;
④甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡.
上述项目中能够说明甲比乙的金属性强的是( )
| A、①② | B、②④ | C、②③ | D、①③ |
下列物质结构的化学用语或模型正确的是( )
| A、乙醇的结构简式:CH3CH2OH |
B、HF的电子式: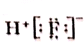 |
C、氯离子的结构示意图: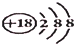 |
D、CH4分子的球棍模型: |
