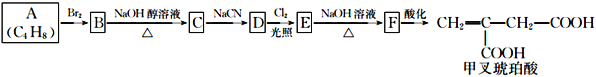
题目内容
【题目】金属钒被誉为“合金的维生素”,常用于催化剂和新型电池。钒(V)在溶液中主要以VO43-(黄色)、VO2+(浅黄色)、VO2+ (蓝色)、V3+(绿色)、V2+(紫色)等形式存在。回答下列问题:
(1)已知:4Al(s)+3O2(g)=2Al2O3(s) △H1 4V(s)+5O2(g)=2V2O5(s) △H2
写出V2O5与Al 反应制备金属钒的热化学方程式__________________。(反应热用△H1、△H2表示)
(2) V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液(含有VO2+),试写出V2O5与浓盐酸
反应的化学反应方程式:_________________________________。
(3)VO43-和V2O74-在pH≥13的溶液中可相互转化。室温下,1.0mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。溶液中c(H+)增大,VO43-的平衡转化率_________(填“增大”“减小”或“不变”)。根据A点数据,计算该转化反应的平衡常数的数值为________。
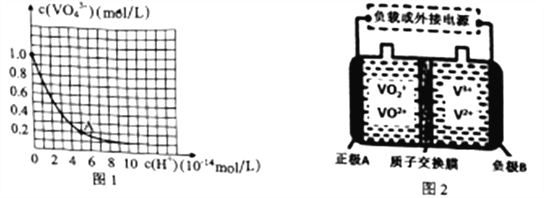
(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图2所示:
①放电过程中,A电极的反应式为___________________。
②充电过程中,B电极附近溶液颜色变化为___________________。
③若该电池放电时的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用率为______________(写出表达式,不必计算出结果。已知:电量Q=It,t为时间/秒;电解时Q=znF,z为每摩尔物质得失电子摩尔数,n为物质的量,法拉弟常数F=96500C/mol,电流利用效率=![]() ×100%)
×100%)
【答案】 10Al(s)+3V2O3(s)=5Al2O3(s)+6V(s) ![]() △H=1/2(5△H1-3△H2) V2O5+6HCl=2VOCl2+Cl2↑+3H2O 增大 0.4 VO2++2H++e-=VO2++H2O 溶液由绿色变为紫色
△H=1/2(5△H1-3△H2) V2O5+6HCl=2VOCl2+Cl2↑+3H2O 增大 0.4 VO2++2H++e-=VO2++H2O 溶液由绿色变为紫色 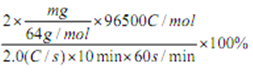
【解析】(1)①4Al(s)+3O2(g)=2Al2O3(s)△H1,②4V(s)+5O2(g)=2V2O5(s)△H2,盖斯定律计算(①×5-②×3)×![]() 得到V2O5与A1反应制备金属钒的热化学方程式10Al(s)+3V2O3(s)=5Al2O3(s)+6V(s)△H=
得到V2O5与A1反应制备金属钒的热化学方程式10Al(s)+3V2O3(s)=5Al2O3(s)+6V(s)△H= ![]() ×(5△H1-3△H2),故答案为:10Al(s)+3V2O3(s)=5Al2O3(s)+6V(s)△H=
×(5△H1-3△H2),故答案为:10Al(s)+3V2O3(s)=5Al2O3(s)+6V(s)△H=![]() ×(5△H1-3△H2)
×(5△H1-3△H2)
(2)V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液为VO2+,V元素化合价+5价变化为+4价,做氧化剂,氯化氢被氧化生成氯气,结合电子守恒、原子守恒配平书写化学方程式V2O5+6HCl=2VOCl2+Cl2↑+3H2O,故答案为:V2O5+6HCl=2VOCl2+Cl2↑+3H2O;
(3)VO43-和V2O74-在pH≥13的溶液中可相互转化,室温下,1.0molL-1的Na3VO4溶液中c(VO43-)随c(H+)的变化,根据图像,氢离子浓度越大,VO43-越少,溶液中Na3VO4转化为Na4V2O7的离子方程式2VO43-+H2OV2O74-+2OH-,由图可知,溶液中c(H+)增大,VO43-的浓度减小,说明VO43-的平衡转化率增大,A点VO43-的浓度为0.2mol/L,消耗浓度1mol/L-0.2mol/L=0.8mol/L,生成的Cr2O72-的浓度为0.4mol/L,此时c(H+)=5×10-14 mol/L,则c(OH-)=0.2 mol/L,K=![]() =0.4,故答案为:增大;0.4;
=0.4,故答案为:增大;0.4;
(4)①放电过程中A电极为原电池正极,电极的反应式为VO2++2H++e-=VO2++H2O,故答案为:VO2++2H++e-=VO2++H2O;
②充电时,右槽B是电解池的阴极,该极上发生得电子的还原反应,即V2+→V3+,应该是绿色变为紫色;故答案为:溶液由绿色变为紫色;
③电解精炼铜得到铜mg时,即铜的物质的量为![]() mol,所以电解消耗的电量Q=2×
mol,所以电解消耗的电量Q=2×![]() mol×96500C/mol,根据放电的电流强度I=2.0A=2.0C/s,电池工作10分钟,可计算得电池的输出电量Q=It=2.0 C/s ×10min×60s/min,所以电流利用效率=
mol×96500C/mol,根据放电的电流强度I=2.0A=2.0C/s,电池工作10分钟,可计算得电池的输出电量Q=It=2.0 C/s ×10min×60s/min,所以电流利用效率=![]() ×100%=
×100%=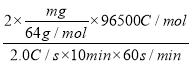 ×100%,故答案为:
×100%,故答案为: 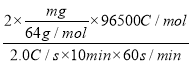 ×100%。
×100%。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】(1)固体可分为晶体、非晶体和准晶体三大类,可通过________________方法区分晶体、非晶体和准晶体,以色列科学家丹尼尔·谢赫特曼因发现锰的化合物准晶体而独享了2011年诺贝尔化学奖。基态Mn原子的电子排布式为_______________。
(2)PCl3的立体构型为______________,中心原子的杂化轨道类型_______________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
BF3 | BCl3 | BBr3 | BI3 | |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是___________________。
②B、C、N、O三种元素第一电离能由小到大的顺序为___________。
③用BF3分子结构解释反应BF3(g)+NH4F(s)=NH4BF4(s)能够发生的原因:____________。
(4)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
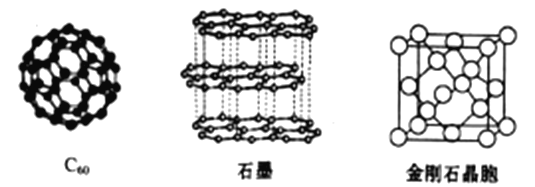
回答下列问题
①石墨晶体中,层内C-C键的键长为142pm,而金刚石中C-C键的键长为154pm,其原因是金刚石中只存在C-C间的________共价键,而石墨层内的C-C间存在_________键。
②金刚石晶胞含有___________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,列式表示碳原子在晶胞中的空间占有率__________(不要求计算结果)。