题目内容
【题目】二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些支持装置省略了)所示。已知SO2Cl2的熔点为-54.1℃,沸点为69. 1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
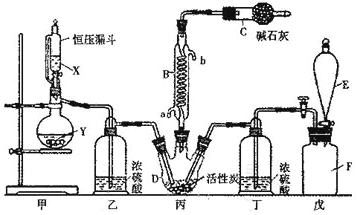
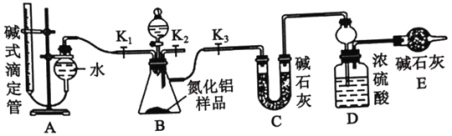
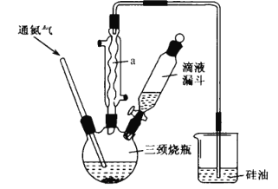
(1)仪器E的名称是_______,由B的使用可知SO2与氯气之间的反应居于______(填“放”或“吸”)热反应,B处反应管冷却水应从___________(填“a”或“b”)接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是__________。
(2)试剂X、Y的组合最好是_________。
a.98%硫酸和铜 b.稀硝酸和亚硫酸钠固体 c.60%硫酸和亚硫酸钾固体
(3)戊是贮气装置,则E中的试剂是_________;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是___________________________.
(4)取1.00g蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.50g,则所得馏分中二氯化砜的质量百分含量为__________%(结果保留小数点后1位)。
(5)二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是______。
【答案】分液漏斗 放 a 该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成 c 饱和食盐水 SO2+ Cl2+2H2O=H2SO4+2HCl 86.9 因为SO2Cl2自身分解生成Cl2, Cl2溶于使液体呈黄色
【解析】
(1)根据装置图可知,E为分液漏斗,因蛇形冷凝管的作用是冷凝回流而反应又没有加热,故SO2与氯气间的反应为放热反应;根据下进上出,的原则,B处反应管冷却水应从a接口通入;由于该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成;故答案为分液漏斗;放;a;该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成;
(2)甲是制备SO2的装置,铜与浓硫酸反应需要加热,硝酸能氧化SO2,所以用c.60% H2SO4+K2SO3来制备SO2,故选c;
(3)因氯水不溶于饱和食盐水,故E中的试剂是饱和食盐水,氯气在水存在的条件下可将SO2氧化成硫酸,自身被还原为HCl,反应的方程式为SO2+Cl2+2H2O=H2SO4+2HCl,故答案为饱和食盐水;SO2+Cl2+2H2O=H2SO4+2HCl;
(4)设所得馏分中二氯化砜的质量百分含量为x,则:
SO2Cl2~H2SO4~BaSO4
135 233
1.00g×x 1.5g
所以135:233=1.00g×x:1.5g
解得x=86.9%
故答案为86.9;
(5)SO2Cl2久置后分解会生成氯气,可能是溶解氯气所致,故答案为二氯化砜久置后分解生成的氯气,溶解在二氯化砜中,使液体呈黄色。

【题目】探究Mg(OH)2的溶解平衡时,利用下表三种试剂进行试验,下列说法中不正确的是( )
编号 | ① | ② | ③ |
分散质 | Mg(OH)2 | HCl | NH4Cl |
备注 | 悬浊液 | 1mol/L | 1mol/L |
A.向①中滴入几滴酚酞试液后,溶液显红色说明Mg(OH)2是一种弱电解质
B.为了使Mg(OH)2悬浊液溶解得更快,加入过量的NH4Cl浓溶液并充分振荡,效果更好
C.①、③混合后发生反应:![]()
D.向①中加入②,H+与OH-反应生成H2O,使c(OH-)减小,Mg(OH)2溶解平衡向溶解方向移动