题目内容
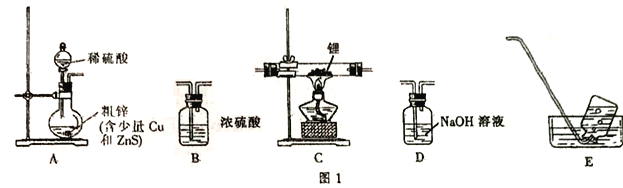
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是

A. 原子半径Y<Z<W
B. 元素Y的最高正化合价比元素X的最高正化合价高
C. 元素W的最高价氧化物对应的水化物的酸性比Q的弱
D. 元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性
【答案】C
【解析】
根据题意X、Y、Z、W、Q分别是N、O、Al、S、Cl。同周期主族元素由左向右原子半径逐渐减小,Y、Z、W的原子半径的大小关系为Z>W>Y,A错误;O元素没有正化合价,B错误;根据“同周金减非递增”规律可知酸性:H2SO4<HClO4,C正确;元素X、Y相比,元素Y形成的简单氢化物较稳定是因为其非金属性强,原子半径小,形成的共用电子对结合牢固,D错误。

练习册系列答案
相关题目
【题目】研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
I.现有反应:①![]() ,②
,②![]() 。
。
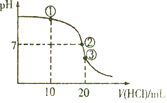
(1)两反应中属于吸热反应的是______![]() 填序号
填序号![]() 。
。
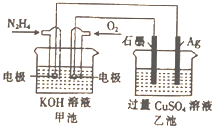
(2)![]() 原电池的装置如图所示。
原电池的装置如图所示。

①溶液中![]() 向______
向______![]() 填“铁”或“铜”
填“铁”或“铜”![]() 电极方向移动。
电极方向移动。
②正极的现象是______,负极的电极反应式为______。
![]() 某可逆反应:
某可逆反应:![]() 在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 |
|
|
|
|
|
| |
2 | 800 |
|
|
|
|
|
|
|
3 | 950 |
|
|
|
|
|
|
|
(3)实验1中,在![]() min内,以物质A表示的平均反应速率为______
min内,以物质A表示的平均反应速率为______![]() ,50min时,
,50min时,![]() 正
正![]() ______
______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 逆
逆![]() 。
。
(4)0~20min内,实验2比实验1的反应速率______![]() 填“快”或“慢”
填“快”或“慢”![]() ,其原因可能是______。
,其原因可能是______。
(5)实验3比实验1的反应速率快,其原因是______。