题目内容
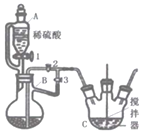
【题目】利用图示实验装置可完成多种实验,其中不能达到相应实验目的的是

选项 | 试剂1、试剂2 | 实验目的 |
A | 过量锌粒、食醋溶液 | 测定食醋中醋酸浓度 |
B | 粗锌、过量稀硫酸 | 测定粗锌(含有不参与反应的杂质)纯度 |
C | 碳酸钠固体、水 | 证明碳酸钠水解吸热 |
D | 过氧化钠固体、水 | 证明过氧化钠与水反应产生气体 |
A.AB.BC.CD.D
【答案】C
【解析】
A.将甲中左侧过量锌粒转移到右侧盛有的一定体积食醋溶液中,测定乙中产生气体体积,可测定酷酸浓度,故A项正确;
B.将甲中右侧过量稀硫酸转移到左侧一定质量的粗锌中,测定己中产生气体体积,可测定粗锌的纯度,B项正确;
C.碳酸钠溶于水的过程中包含溶解和水解,水解微弱、吸收热量少,溶解放热,且放出热量大于吸收的热量,故C项错误;
D.过氧化钠与水反应放热并产生氧气,恢复至室温后,可根据己中两侧液面高低判断是否有气体产生,故D项正确;
故答案为C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目