题目内容
18.某溶液中含有X-、Y2-、Z2-三种常见的无机离子.如图所示,发生了一系列化学反应.第④步反应生成的白色沉淀中含Y2-.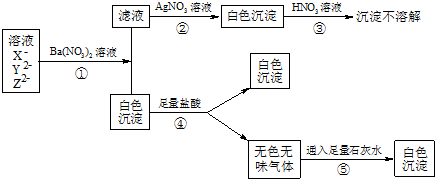
(1)判断X-、Y2-、Z2-分别为Cl-、SO42-(CO32-)、CO32-(SO42-)(写离子符号).
(2)写出④、⑤步反应的离子方程式.
④BaCO3+2H+=Ba2++CO2+H2O;
⑤CO2+2OH-+Ca2+=CaCO3+H2O.
分析 溶液中加入硝酸钡后产生白色沉淀,白色沉淀中加入盐酸沉淀部分溶解,说明沉淀中含有硫酸钡和碳酸钡,碳酸钡与盐酸反应能产生无色无味的气体二氧化碳,二氧化碳与石灰水反应能生成白色沉淀碳酸钙,故溶液中含有硫酸根离子和碳酸根离子;滤液中加入硝酸银产生不溶于硝酸的白色沉淀,说明溶液中含有氯离子,氯离子与银离子结合生成氯化银不溶于硝酸.据此分析解答.
解答 解:溶液中加入硝酸钡后产生白色沉淀,白色沉淀中加入盐酸沉淀部分溶解,说明沉淀中含有硫酸钡和碳酸钡,碳酸钡与盐酸反应能产生无色无味的气体二氧化碳,二氧化碳与石灰水反应能生成白色沉淀碳酸钙,故溶液中含有硫酸根离子和碳酸根离子;滤液中加入硝酸银产生不溶于硝酸的白色沉淀,说明溶液中含有氯离子,氯离子与银离子结合生成氯化银不溶于硝酸;
(1)由上述分析可知X-为氯离子,Y2-和Z2-为硫酸根离子和碳酸根离子,符号分别为 Cl-、SO42-、CO32-;
故答案为:Cl-;SO42-(CO32-);CO32-(SO42-);
(2)④反应为盐酸中的氢离子与碳酸钡反应生成二氧化碳的过程,离子方程式为BaCO3+2H+═Ba2++CO2↑+H2O;
⑤步反应为二氧化碳与石灰水反应,离子方程式Ca2++2OH-+CO2═CaCO3↓+H2O,
故答案为:BaCO3+2H+=Ba2++CO2+H2O;CO2+2OH-+Ca2+=CaCO3+H2O.
点评 本题考查无机物的推断,侧重于考查学生的综合分析能力,把握白色沉淀及离子之间的反应逐一分析推断为解答的关键,题目难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
8.下列化学反应能用离子方程式H+十OH-=H2O来表示的是( )
| A. | 盐酸和氢氧化铜 | B. | 硫酸和氢氧化钠溶液 | ||
| C. | 硫酸和氢氧化钡溶液 | D. | 稀硝酸和氨水混合 |
9.下列离子方程式书写正确的是( )
| A. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| B. | NH4HCO3溶液与足量NaOH溶液混合加热:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO32-+2H2O | |
| C. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
3.通常状况下下列气体遇到空气会发生颜色变化的是( )
| A. | N2 | B. | NH3 | C. | CO2 | D. | NO |
10.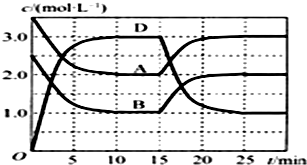 温度为T时,向V L的密闭容器中充入一定量的气体A和B,发生反应:A(g)+B(g)?C(s)+x D(g);△H>0,反应过程中容器内A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )
温度为T时,向V L的密闭容器中充入一定量的气体A和B,发生反应:A(g)+B(g)?C(s)+x D(g);△H>0,反应过程中容器内A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )
 温度为T时,向V L的密闭容器中充入一定量的气体A和B,发生反应:A(g)+B(g)?C(s)+x D(g);△H>0,反应过程中容器内A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )
温度为T时,向V L的密闭容器中充入一定量的气体A和B,发生反应:A(g)+B(g)?C(s)+x D(g);△H>0,反应过程中容器内A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )| A. | 该反应的平衡常数表达式K=$\frac{c(C)•{c}^{2}(D)}{c(A)•c(B)}$ | |
| B. | 若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动 | |
| C. | 反应至15 min时,改变的条件是升高温度 | |
| D. | 反应在前10 min的平均反应速率:v(D)=0.3 mol•L-1•min-1 |
4. 如图锥形瓶中装满了c mol•Lˉ1的Na2SO4溶液,经测定其中含有a mol Na+,则锥形瓶容
如图锥形瓶中装满了c mol•Lˉ1的Na2SO4溶液,经测定其中含有a mol Na+,则锥形瓶容
积为( )
 如图锥形瓶中装满了c mol•Lˉ1的Na2SO4溶液,经测定其中含有a mol Na+,则锥形瓶容
如图锥形瓶中装满了c mol•Lˉ1的Na2SO4溶液,经测定其中含有a mol Na+,则锥形瓶容积为( )
| A. | $\frac{a}{c}$ L | B. | $\frac{a}{2c}$L | C. | ac L | D. | 2ac L |