题目内容
9.下列离子方程式书写正确的是( )| A. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| B. | NH4HCO3溶液与足量NaOH溶液混合加热:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO32-+2H2O | |
| C. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
分析 A.石灰乳中氢氧化钙应保留化学式;
B.二者反应生成氨气、碳酸钠和水;
C.醋酸铵为强电解质,应拆成离子形式;
D.离子个数配比不符合物质结构.
解答 解:A.石灰乳与Na2CO3溶液混合,离子方程式:Ca(OH)2+CO32-═CaCO3↓+2OH-,故A错误;
B.NH4HCO3溶液与足量NaOH溶液混合加热,离子方程式:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO32-+2H2O,故B正确;
C.氨气通入醋酸溶液,离子方程式:CH3COOH+NH3═CH3COO-+NH4+,故C错误;
D.氢氧化钡溶液与稀硫酸反应,离子方程式:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O,故D错误;
故选:B.
点评 本题考查离子反应方程式的书写,明确反应实质是解题关键,注意化学式的拆分,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
相关题目
19.下列叙述正确的是( )
| A. | 1.00molNaCl中含有6.02×1023个 NaCl 分子 | |
| B. | 1.00molNaCl中,所有Na+的最外层电子总数为8×6.02×1023 | |
| C. | 欲配制1.00L 1.00 mol•L-1的 NaCl 溶液,可将58.5gNaCl溶于1.00L水中 | |
| D. | 电解58.5g熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
20.下列离子方程式中,只能表示一个化学反应的是( )
①CO32-+2H+═CO2↑+H2O
②Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
③Ag++Cl-═AgCl↓
④Fe+Cu2+═Fe2++Cu.
①CO32-+2H+═CO2↑+H2O
②Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
③Ag++Cl-═AgCl↓
④Fe+Cu2+═Fe2++Cu.
| A. | ①③ | B. | ②④ | C. | ②③ | D. | 没有 |
17.下列说法正确的是( )
| A. | 摩尔是一种国际基本物理量 | |
| B. | 在同温同压下,相同体积的任何气体单质所含分子数相同 | |
| C. | 标准状况下气体摩尔体积约为22.4 L | |
| D. | 1 mol氧的质量为16 g |
14.有下列两个反应:①Cl2+2NaBr═2NaCl+Br2②Co2O3+6HCl═2CoCl2+Cl2↑+3H2O下列说法正确的是( )
| A. | 反应①②中的氧化产物分别是Br2、CoCl2 | |
| B. | 根据以上方程式可以得到氧化性:Cl2>Br2>Co2O3 | |
| C. | 通过推理得到:Co2O3不能与HBr溶液发生氧化还原反应生成Br2 | |
| D. | 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
1.下列陈述I、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述Ⅱ |
| A | SO2和氯水有漂白性 | 两者都能使溴水褪色 |
| B | CuSO4可以用作游泳池消毒剂 | 铜盐能使蛋白质变性 |
| C | 盐酸和氨水能溶解Al(OH)3 | Al(OH)3是两性氢氧化物 |
| D | 用淀粉-KI溶液鉴别FeCl2 | Fe2+有氧化性 |
| A. | A | B. | B | C. | C | D. | D |
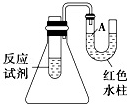 (1)如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:
(1)如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题: