题目内容
1.(1)A、B为同周期第IIA和第IVA元素,若它们处在第三周期,则原子序数之差为2.若它们处在第四周期,则原子序数之差为12.若它们处在第六周期,则原子序数之差为26.(2)A元素所处周期有m种元素,B元素所处周期有n种元素,若A、B都为IA族元素且A在B的上一周期,A的原子序数为x,则B的原子序数为x+m.若A、B都为VIIA族元素且A在B的下一周期,A的原子序数为x,则B的原子序数为x-m.
分析 (1)A、B为同周期第IIA和第IVA元素,若它们处在第三周期,A、B分别为Mg、Si;若它们处在第四周期,中间相隔12个纵行(含副族和第ⅤⅢ);若它们处在第六周期,含錒系;
(2)若A、B都为IA族元素且A在B的上一周期,原子序数之差为上一周期元素的种类数;若A、B都为VIIA族元素且A在B的下一周期,原子序数之差为下一周期元素的种类数.
解答 解:(1)A、B为同周期第IIA和第IVA元素,若它们处在第三周期,A、B分别为Mg、Si,则A、B的原子序数之差为2;若它们处在第四周期,中间相隔12个纵行(含副族和第ⅤⅢ),则A、B的原子序数之差为12;若它们处在第六周期,含錒系,则A、B的原子序数之差为26,
故答案为:2;12;26;
(2)若A、B都为IA族元素且A在B的上一周期,原子序数之差为上一周期元素的种类数,A的原子序数为x,A元素所处周期有m种元素,则B的原子序数为x+m;若A、B都为VIIA族元素且A在B的下一周期,原子序数之差为下一周期元素的种类数,A的原子序数为x,A元素所处周期有m种元素,则B的原子序数为x-m,
故答案为:x+m;x-m.
点评 本题考查元素周期律的结构及应用,为高频考点,把握元素的位置、原子序数的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
17.某溶液中大量存在的五种离子:NO3-、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M可能为( )
| A. | Na+ | B. | Mg2+ | C. | CO32- | D. | Ba2+ |
12.除去某溶液里溶解的少量杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A. | KNO3溶液(AgNO3):加过量KCl溶液,过滤 | |
| B. | NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热 | |
| C. | NaCl溶液(Br2):加CCl4,萃取分液 | |
| D. | KNO3溶液(NaCl):加热蒸发得浓溶液后,降温 |
16.下列说法正确的是( )
| A. | 炒过菜的铁锅不及时清洗易生锈 | |
| B. | 轮船吃水线以下的船壳外焊上锌块,可以防止铁船体被腐蚀 | |
| C. | 铁发生电化学腐蚀时铁为正极 | |
| D. | 经常用钢丝球擦洗铝锅表面,可以防止铝锅被腐蚀 |
13.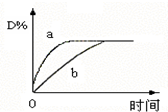 已知反应:3A(g)+B(g)?C(s)+4D(g)△H<0.图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况.若使曲线b变为曲线a,可采取的措施是( )
已知反应:3A(g)+B(g)?C(s)+4D(g)△H<0.图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况.若使曲线b变为曲线a,可采取的措施是( )
 已知反应:3A(g)+B(g)?C(s)+4D(g)△H<0.图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况.若使曲线b变为曲线a,可采取的措施是( )
已知反应:3A(g)+B(g)?C(s)+4D(g)△H<0.图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况.若使曲线b变为曲线a,可采取的措施是( )| A. | 升高温度 | B. | 减小B的浓度 | ||
| C. | 增加C质量 | D. | 缩小反应容器的体积 |
10.以下反应的反应类型,其中一个不同于其他三个的是( )
| A. | 在光照条件下,甲烷与足量氯气反应生成四氯化碳 | |
| B. | 在溴化铁催化剂作用下,苯与溴反应生成溴苯 | |
| C. | 乙醇在铜或银作催化剂的条件下,与空气中的氧气反应生成乙醛 | |
| D. | 乙酸与乙醇在浓硫酸的作用下生成不溶于水的油状液体 |
11.下列反应中属于加成反应的是( )
| A. | CH3CH3+2Cl2$\stackrel{光}{→}$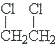 +2HCl +2HCl | B. | CH2=CH-CH=CH2+Br2→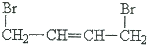 | ||
| C. | 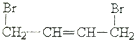 +2NaOH$→_{△}^{水}$ +2NaOH$→_{△}^{水}$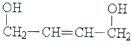 +2NaBr +2NaBr | D. |  $→_{△}^{浓硫酸}$CH2=CHCH2CH3↑+H2O $→_{△}^{浓硫酸}$CH2=CHCH2CH3↑+H2O |
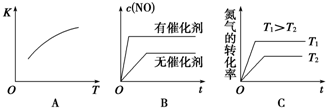 汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0,已知该反应在2 404℃,平衡常数K=64×10-4.请回答:
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0,已知该反应在2 404℃,平衡常数K=64×10-4.请回答: ,B原子L层的电子总数是K层的3倍;0.1mol C单质能从酸中置换出2.24L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同.
,B原子L层的电子总数是K层的3倍;0.1mol C单质能从酸中置换出2.24L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同.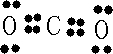 .
.