题目内容
【题目】![]() 作为一种重要的化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究着被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
作为一种重要的化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究着被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应Ⅰ:![]()
![]()
![]() △H=
△H=![]()
反应Ⅱ:![]()
![]()
![]()
![]()
(1)在恒温恒容装置中充入一定量的![]() 和
和![]() ,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是___________________。
,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是___________________。
A. 使用催化剂时,可降低该反应的活化能,加快其反应速率
B. 若测得容器内![]() 时,说明反应已达平衡
时,说明反应已达平衡
C. 当容器内![]() 时,说明反应已达平衡
时,说明反应已达平衡
D. 当测得容器内氧气浓度不再变化时,说明反应已达达平衡
(2)氨催化氧化时会发生上述两个竞争反应Ⅰ、Ⅱ。为分析某催化剂对该反应的选择性,1L密闭容器中充入1 mol ![]() 和2 mol
和2 mol ![]() ,测得有关物质的量关系如图
,测得有关物质的量关系如图
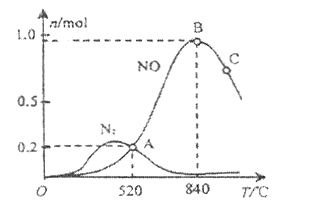
①该催化剂在高温时选择反应_______________(填“Ⅰ”或“Ⅱ”)。
②520℃时, ![]()
![]()
![]() 的平衡常数K表达式________。
的平衡常数K表达式________。
③有利于提高![]() 转化为
转化为![]() 的速率的措施有_________________。
的速率的措施有_________________。
A. 使用催化剂![]()
B. 将反应生成的![]() 及时移出
及时移出
C. 充入稀有气体
D. 投料比不变,增加反应物的浓度
E. 降低反应温度
(3)最近华南理工大提出利用电解法制![]() 并用产生的
并用产生的![]() 处理废氨水,装置如图
处理废氨水,装置如图
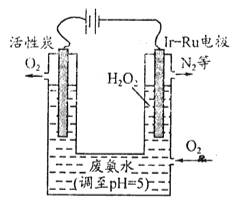
①为了不影响![]() 的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)_________c(NO3-)(填>、=、<)。
的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)_________c(NO3-)(填>、=、<)。
②Ir-Ru惰性电极有吸附![]() 作用,该电极上产生
作用,该电极上产生![]() 的反应为_________,生成的
的反应为_________,生成的![]() 与废液反应的离子方程式为_________________。
与废液反应的离子方程式为_________________。
③理论上电路中每转移3 mol电子,最多可以处理![]() 的物质的量为__________。
的物质的量为__________。
【答案】 A、D I ![]() A、D <
A、D < ![]()
![]() 1 mol
1 mol
【解析】(1)A.加入催化剂,改变反应途径,降低反应的活化能,增加了活化分子百分数,化学反应速率增大,选项A正确;B.对于反应![]()
![]()
![]() ,应是 6v 正(NH3)=4v 逆(H2O)时,反应达到平衡状态,选项B错误;C.当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,与
,应是 6v 正(NH3)=4v 逆(H2O)时,反应达到平衡状态,选项B错误;C.当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,与 ![]() 无关,选项C错误;D. 反应进行时,氧气的浓度在变化,当测得容器内氧气浓度不再变化时,说明反应已达达平衡,选项D正确。答案选AD;(2)①由图可知,该催化剂在高温时,生成的NO物质的量远大于氮气的,故该催化剂在高温下选择反应I;②
无关,选项C错误;D. 反应进行时,氧气的浓度在变化,当测得容器内氧气浓度不再变化时,说明反应已达达平衡,选项D正确。答案选AD;(2)①由图可知,该催化剂在高温时,生成的NO物质的量远大于氮气的,故该催化剂在高温下选择反应I;②![]()
![]()
![]() 的平衡常数K表达式
的平衡常数K表达式 ;③A.使用催化剂能加快反应速率,缩短到达平衡的时间,选项A正确;B.将反应生成的
;③A.使用催化剂能加快反应速率,缩短到达平衡的时间,选项A正确;B.将反应生成的![]() 及时移出,生成物浓度降低,反应速率减小,选项B错误;C.恒容条件下充入稀有气体,降低反应物的浓度,反应速率减小,选项C错误;D.投料比不变,增加反应物的浓度,反应速率增大,选项D正确;E.降低温度,反应速率减慢,选项E错误。答案选AD;(3)①向废氨水加入适量硝酸调节溶液的pH约为5,根据溶液呈电中性,溶液中c(NH4+)+c(H+)=c(NO3-)+c(OH-),pH约为5呈酸性,c(H+)>c(OH-),所以c(NH4+)<c(NO3-);②利用电解法制H2O2,在该电解池中,Ir-Ru惰性电极有吸附O2作用为氧气得电子发生还原反应,
及时移出,生成物浓度降低,反应速率减小,选项B错误;C.恒容条件下充入稀有气体,降低反应物的浓度,反应速率减小,选项C错误;D.投料比不变,增加反应物的浓度,反应速率增大,选项D正确;E.降低温度,反应速率减慢,选项E错误。答案选AD;(3)①向废氨水加入适量硝酸调节溶液的pH约为5,根据溶液呈电中性,溶液中c(NH4+)+c(H+)=c(NO3-)+c(OH-),pH约为5呈酸性,c(H+)>c(OH-),所以c(NH4+)<c(NO3-);②利用电解法制H2O2,在该电解池中,Ir-Ru惰性电极有吸附O2作用为氧气得电子发生还原反应, ![]() ;生成的
;生成的![]() 与废液反应的离子方程式为
与废液反应的离子方程式为![]() ;③4NH3+3O22N2+6H2O中,氨气中的氮元素从-3价变为氮气中的0价,4mol氨气转移12mol电子,所以转移3mol电子,最多可以处理NH3H2O的物质的量为1mol。
;③4NH3+3O22N2+6H2O中,氨气中的氮元素从-3价变为氮气中的0价,4mol氨气转移12mol电子,所以转移3mol电子,最多可以处理NH3H2O的物质的量为1mol。

【题目】“中和滴定”原理在实际生产生活中应用广泛。用I2O5可定量测定CO的含量,该反应原理为5CO+I2O5![]() 5CO2+I2。其实验步骤如下:
5CO2+I2。其实验步骤如下:
①取250 mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管中在170 ℃下充分反应;
②用水一乙醇液充分溶解产物I2,配制100 mL溶液;
③量取步骤②中溶液25.00 mL于锥形瓶中,然后用0.01 mol·L-1的Na2S2O3标准溶液滴定。消耗标准Na2S2O3溶液的体积如表所示。
第一次 | 第二次 | 第三次 | |
滴定前读数/mL | 2.10 | 2.50 | 1.40 |
滴定后读数/mL | 22.00 | 22.50 | 21.50 |
(1)步骤②中配制100 mL待测溶液需要用到的玻璃仪器的名称是烧杯、量筒、玻璃棒、胶头滴管和____________________。
(2)Na2S2O3标准液应装在__________(填字母)中。

(3)指示剂应选用__________,判断达到滴定终点的现象是____________________________________。
(4)气体样品中CO的体积分数为__________(已知:气体样品中其他成分不与I2O5反应:2Na2S2O3+I2=2NaI+Na2S4O6)
(5)下列操作会造成所测CO的体积分数偏大的是__________(填字母)。
a.滴定终点俯视读数
b.锥形瓶用待测溶液润洗
c.滴定前有气泡,滴定后没有气泡
d.配制100 mL待测溶液时,有少量溅出