题目内容
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
②H2O(l) H2O(g) △H="+" 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
(2)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。

①在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂。
②能判断该反应在“图2”所在条件下是否已达化学平衡状态的依据是 。(双选)
③计算该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数K= 。
CH3OH(g)的化学平衡常数K= 。
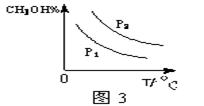
④请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(3)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6。现将c mol·L-1 CaCl2溶液与2.00×10-2 mol·L-1 Na2SO4溶液等体积混合生成沉淀,则c的最小值是 (结果保留3位有效数字)。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)
②H2O(l)
写出表示甲醇燃烧热的热化学方程式 。
(2)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
①在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂。
②能判断该反应在“图2”所在条件下是否已达化学平衡状态的依据是 。(双选)
| A.容器中压强不变 | B.体系的密度不随时间改变 |
| C.v正(H2)=2v逆(CH3OH) | D.CO与H2的物质的量的比不随时间改变 |
 CH3OH(g)的化学平衡常数K= 。
CH3OH(g)的化学平衡常数K= 。④请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(3)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6。现将c mol·L-1 CaCl2溶液与2.00×10-2 mol·L-1 Na2SO4溶液等体积混合生成沉淀,则c的最小值是 (结果保留3位有效数字)。
(16分)
(1)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) △H=—725.8kJ/mol (共3分,化学方程式1分,△H 2分。如果甲醇的系数不是1扣2分,状态符号不全扣1分,△H漏单位扣1分)
(2)①b(2分)②AC(2分,全对2分,选对1
个得1分,有错得0分。)
③ 12(3分,有单位且正确也给分)
④(3分,全对才得分,不标P1、P2不给分)
(3)1.82×10-3(3分,多写单位不扣分,有效数字错扣1分)
(1)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) △H=—725.8kJ/mol (共3分,化学方程式1分,△H 2分。如果甲醇的系数不是1扣2分,状态符号不全扣1分,△H漏单位扣1分)
(2)①b(2分)②AC(2分,全对2分,选对1
个得1分,有错得0分。)
③ 12(3分,有单位且正确也给分)
④(3分,全对才得分,不标P1、P2不给分)

(3)1.82×10-3(3分,多写单位不扣分,有效数字错扣1分)
试题分析:(1)依题意,根据盖斯定律和燃烧热的定义,由①/2—②×2可得:CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) △H=—725.8kJ/mol;(2)①读图,曲线a、b表示活化能不同,说明b使用了催化剂,降低该反应的活化能;②正反应是气体物质的量增大的方向,未达平衡时容器中混合气体总的物质的量增大,因此压强增大,若压强不变,说明各组分物质的量不变,即达到平衡,故A正确;由于混合气体的密度等于混合气体的总质量除以密闭容器的容积,由于各组分都是气体,根据质量守恒定律推断混合气体的总质量始终不变,因此密度不变不能说明达到平衡,故B错误;用不同物质表示的正、逆反应速率之比等于化学方程式中的系数之比,说明达到平衡,故C正确;各组分的物质的量不随时间改变能说明达到平衡,但两反应物的物质的量之比不随时间改变,则不能说明达到平衡,故D错误;③由读图可推断该反应中各组分(起始、变化、平衡)浓度,则:
CO(g) + 2H2(g)
 CH3OH(g)
CH3OH(g)起始浓度/ mol?Lˉ1 1.00 2.00 0
变化浓度/ mol?Lˉ1 0.75 1.50 0.75
平衡浓度/ mol?Lˉ1 0.25 0.50 0.75
K=c(CH3OH)/[c(CO)?c2(H2))]=" 0.75/[" 0.25××0.502]=12
④正反应是气体体积减小的反应,根据化学反应自发进行的规律推断,逆反应能自发进行的原因是符合熵判据,正反应能自发的原因是符合焓判据,所以正反应是放热反应,其它条件不变时,升高温度平衡向逆反应方向移动,甲醇百分含量减小;增大压强平衡向正反应方向移动,甲醇百分含量增大;因此画图要点是:P1、P2时甲醇百分含量都随温度升高逐渐减小,P2时甲醇百分含量—温度曲线高于P1;
(3)两溶液混合导致相互稀释,根据稀释定律:c1?V1=c2?V2,则混合后氯化钙和硫酸钠溶液的浓度都要减半;因此钙离子浓度为c/2 mol·L-1,硫酸根离子浓度为1.00×10-2 mol·L-1,由于Ksp(CaSO4)=c(Ca2+)?c(SO42-),则c/2×1.00×10-2=9.10×10-6,即c=1.82×10-3;根据溶度积规则,只有Qc(CaSO4)> Ksp(CaSO4)时,才能形成硫酸钙的过饱和溶液,才有沉淀析出,则c最小值为1.82×10-3。

练习册系列答案
相关题目


 2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能为EbkJ·mol-1,则△H =(Ea-Eb)kJ·mol-1。其归纳正确的是
2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能为EbkJ·mol-1,则△H =(Ea-Eb)kJ·mol-1。其归纳正确的是 ,下列叙述中不正确的是
,下列叙述中不正确的是