题目内容
【题目】我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
Ⅰ.已知:2CO(g) + O2(g) = 2CO2(g) △ H = 566kJ/mol;2Fe(s)+![]() O2(g)= Fe2O3(s) △ H = 825.5kJ/mol
O2(g)= Fe2O3(s) △ H = 825.5kJ/mol
反应:Fe2O3(s) + 3CO(g)![]() 2Fe(s) + 3CO2(g) △H =_____kJ/mol。
2Fe(s) + 3CO2(g) △H =_____kJ/mol。
Ⅱ.反应 Fe2O3(s) + 3CO(g)![]() 2Fe(s) + 3CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。
2Fe(s) + 3CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。
(1)欲提高 CO 的平衡转化率,促进 Fe2O3的转化,可采取的措施是_____
a.提高反应温度 b.增大反应体系的压强 c.选取合适的催化剂 d.及时吸收或移出部分CO2 e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:
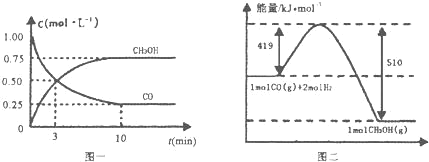
CO(g) + 2H2(g)![]() CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2) =_____。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1,Q2,Q3均大于 0) |
甲 | 1mol CO 和 2mol H2 | a1 | c1 | 放出Q1kJ 热量 |
乙 | 1mol CH3OH | a2 | c2 | 吸收Q2kJ 热量 |
丙 | 2mol CO 和 4mol H2 | a3 | c3 | 放出Q3kJ 热量 |
则下列关系正确的是_____。
a. c1 = c2 b..2Q1 = Q3 c..2a1 = a3 d..a1+ a2= 1 e.该反应若生成1mol CH3OH,则放出(Q1 + Q2)kJ 热量
【答案】-23.5 d ![]() ade
ade
【解析】
I. 依据热化学方程式和盖斯定律计算得到需要的热化学方程式;
II.(1)提高CO的平衡转化率,应使平衡向正反应移动,但不能增大CO的用量;
III.(1)根据图象中生成甲醇的物质的量浓度,求出消耗的氢气的物质的量浓度,再求出氢气的反应速率;
(2)甲容器反应物投入1molCO,2molH2与乙容器反应物投入1mol CH3OH在保持恒温、恒容情况下是等效平衡;甲容器反应物投入量1molCO、2molH2与丙容器反应物投入量2molCO、4molH2,丙中反应物的物质的量为甲的2倍,压强增大,丙容器平衡向正向移动。
Ⅰ.①2CO(g) + O2(g) = 2CO2(g) ΔH = 566kJ/mol;②2Fe(s)+![]() O2(g)= Fe2O3(s) ΔH = 825.5kJ/mol;盖斯定律:①
O2(g)= Fe2O3(s) ΔH = 825.5kJ/mol;盖斯定律:①![]() -②得:Fe2O3(s) + 3CO(g)
-②得:Fe2O3(s) + 3CO(g)![]() 2Fe(s) + 3CO2(g) ΔH = 566kJ/mol
2Fe(s) + 3CO2(g) ΔH = 566kJ/mol![]() +825.5kJ/mol=-23.5 kJ/mol,故答案为:-23.5。
+825.5kJ/mol=-23.5 kJ/mol,故答案为:-23.5。
Ⅱ.(1)a.该反应正反应是放热反应,升高温度,平衡逆向移动,CO的平衡转化率降低,a错误;
b.反应前后气体的物质的量不变,增大压强,平衡不移动,CO的平衡转化率不变,b错误;
c.加入合适的催化剂,平衡不移动,c错误;
d.移出部分CO2,平衡正向移动,CO的平衡转化率增大,d正确;
e.粉碎矿石,使其与平衡混合气体充分接触,反应速率增大,但平衡不移动,e错误;故答案为:d。
Ⅲ.(1)达到平衡时生成甲醇为0.75mol/L,则消耗的c(H2)=2×0.75mol/L=1.5mol/L,![]() ,故答案为:
,故答案为:![]() 。
。
(2)a. 甲、乙相比较,把乙等效为开始加入1mol CO和2mol H2,和甲是等效的,甲乙是等效平衡,所以平衡时甲醇的浓度c1=c2,a正确;
b. 甲、丙相比较,丙中反应物的物质的量为甲的2倍,压强增大,对于反应CO(g)+2H2(g)CH3OH(g),平衡向生成甲醇的方向移动,所以2Q1<Q3,b错误;
c. 甲、丙相比较,丙中反应物的物质的量为甲的2倍,压强增大,对于反应CO(g)+2H2(g)CH3OH(g),平衡向生成甲醇的方向移动,所以a1<a3 ,c错误;
d. 甲、乙处于相同的平衡状态,反应方向相反,则α1+α2=1,d正确;
e. 甲、乙处于相同的平衡状态,反应方向相反,两个方向转化的和恰好为1mol,所以该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量,e正确;故答案为:ade。

 阅读快车系列答案
阅读快车系列答案【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是______(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是____(填字母)。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)c(OH﹣) D.c(OH-)/c(H+) E.![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:___________。
(4)25℃时,将a mol/L的醋酸与b mol/L氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为_____。
(5)标准状况下,将1.12L CO2通入100mL 1mol/L的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: c(OH-)=2c(H2CO3)+___。
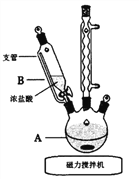
【题目】Ⅰ.中和热的测定是高中重要的定量实验。取50mL 0.55mol/L的NaOH溶液与50mL 0.25mol/L的硫酸溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:

(1)仪器A的名称是____________。
(2)实验测得的数据如下表:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4 |
2 | 25.9 | 25.9 | 25.9 | 29.2 | |
3 | 26.4 | 26.2 | 26.3 | 29.8 | |
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。ΔH=__________ ( 取小数点后一位)。
(3)若改用60mL 0.25mol·L-1H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量______,若实验操作均正确,则所求中和热_____。
II、某课外活动小组拟探究H+浓度对MnO2与H2O2反应速率的影响。
(4)现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间。
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
水的体积/mL | 15 | 14.5 | V4 | 13.5 |
所需时间t/s | t1 | t2 | t3 | t4 |
已知酸条件下时:MnO2+H2O2+2H+=Mn2++O2↑+2H2O
①实验I发生反应的化学方程式为 ________,实验II中MnO2的作________。
②上表中V1=_______mL,V3=_______mL。
③若实验测得t2>t3>t4,则可得出的实验结论是______。