题目内容
【题目】下列有关实验装置正确且能达到实验目的的是( )
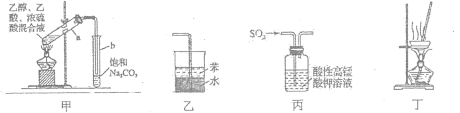
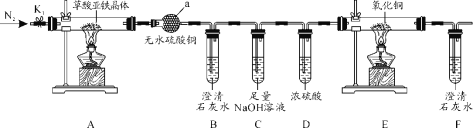
A.用图甲所示装置制取少量乙酸乙酯
B.用图乙所示装置吸收氨气防倒吸
C.用图丙所示装置验证SO2的漂白性
D.用图丁所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
【答案】A
【解析】
A.乙醇和乙酸在浓硫酸的作用下发生酯化反应生成乙酸乙酯,利用饱和碳酸钠溶液吸收乙酸乙酯,图甲所示装置可以制取少量乙酸乙酯,A正确;
B.氨气极易溶于水,导管直接插入水中容易倒吸,用图乙所示装置吸收氨气不能防倒吸;B错误;
C.酸性高锰酸钾溶液具有强氧化性,用图丙所示装置验证SO2的是还原性,C错误;
D.氯化铵受热易分解,不能用图丁所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体,D错误;
答案选A。

练习册系列答案
相关题目