题目内容
2.下列有机化学方程式书写完全正确的是( )| A. | TNT的制备: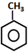 +3HNO3$→_{100℃}^{浓硫酸}$ +3HNO3$→_{100℃}^{浓硫酸}$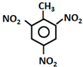 +3H2O +3H2O | |
| B. | 溴乙烷的消去反应:C2H3Br+NaOH$→_{△}^{水}$C2H4↑+NaBr+H2O | |
| C. | 乙醇氧化成乙醛:2C2H5OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O | |
| D. | 乙酸乙酯在碱性条件下水解:CH3COOC2H5+H2O$?_{△}^{碱性}$CH3C0OH+C2H5OH |
分析 A.甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯,三硝基甲苯不存在碳氧键,结构简式错误;
B.溴乙烷在氢氧化钠的醇溶液中发生消去反应,消去反应条件错误;
C.乙醇在铜或银催化作用下加热生成乙醛;
D.乙酸乙酯在碱性条件下完全水解,水解生成乙酸钠和乙醇.
解答 解:A.三硝基甲苯不存在碳氧键,结构简式错误,甲苯可以和浓硝酸之间发生取代反应生成2,4,6-三硝基甲苯,即TNT,化学反应方程式为 ,故A错误;
,故A错误;
B.溴乙烷与氢氧化钠的醇溶液共热发生消去反应,生成乙烯和溴化钠,水;反应的化学方程式为:CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O,故B错误;
C.乙醇中含-OH,能发生催化氧化生成乙醛,该反应方程式为:2C2H5OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,故C正确;
D.乙酸乙酯在碱性条件下的水解方程式是:CH3COOC2H5+NaOH→CH3COONa+C2H5OH,故D错误;
故选C.
点评 本题考查了有机化学反应方程式的书写,注意掌握相关官能团的性质以及有机化合物的断键部位,注意发生的反应类型,题目难度不大.

练习册系列答案
相关题目
3.下列说法不正确的是( )
| A. | CF4、CCl4、CBr4、CI4的熔点沸点升高与范德华力有关 | |
| B. | H2O的熔、沸点大于H2S的是由于H2O之间存在氢键 | |
| C. | 乙醇与水互溶可以用相似相溶原理解释 | |
| D. | 分子晶体中分子一定紧密堆积 |
10. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
(1)①写出工业合成氨的化学方程式N2+3H2$?_{高温高压}^{催化剂}$2NH3.
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a molH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a molH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
17.截止2015年5月25日,据世界卫生组织(WHO)公布的数据显示,全球累计实验室确诊的感染MERS-CoV病例(即中东呼吸综合症,简称MERS)共1139例,其中431例死亡(病死率37.8%).这种新型冠状病毒名称定为“中东呼吸系统综合征冠状病毒”,关于此病毒下列说法正确的是( )
| A. | 该病毒主要通过血液向他人传染 | |
| B. | 该病毒在浓盐溶液中一定会发生变性 | |
| C. | 通常将病毒样本保存在福尔马林中 | |
| D. | 该病毒在一定条件下水解最终会生成氨基酸 |
7.下列叙述不正确的是( )
| A. | 乙烯、油脂、天然橡胶和蛋白质分子中均含有双键 | |
| B. | 相同物质的量的甲基、羟基或氨基所含的电子数目相同 | |
| C. | 常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数不为定值 | |
| D. | 利用红外光谱仪记录的红外光谱图可以初步推测有机化合物中官能团的类别 |
14.复分解反应是中学化学中常见的一种反应类型.
请回答下列问题.
(1)已知在常温下测得浓度均为0.1mol•L-1的下列6种溶液的pH:
复分解反应在这样一个规律:一种较强酸与另一种较弱酸的盐可自发地反应,生成较弱酸
和较强酸的盐,如:2CH3COOH+Na2CO3═2CH3COONa+CO2↑+H2O,若换个角度看,它同时揭示出另一条
规律:碱性较强的物质发生类似反应可以生成碱性较弱的物质.依照该规律,请判断下列反应不能发生的是AD(填编号).
A.CO2+H2O+2NaClO→Na2CO3+2HClO
B.CO2+H2O+NaClO→NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
(2)得根据前述信息判断,常温下,浓度均为0.05mol/L的下列5种物质的溶液中,pH最小的是⑤(填编号),其pH=1(填数值);pH最大的是①(填编号)
①C6H5OH②CH3COOH③HClO4④HClO⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律,下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性的钠溶液;
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体.
请根据上述反应,总结出复分解反应的另一规律:复分解反应能向着生成更难溶物质的方向进行.
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可以观察到的现象是白色固体变为黄色,反应的离子方程式为I-+AgCl=AgI+Cl-.
请回答下列问题.
(1)已知在常温下测得浓度均为0.1mol•L-1的下列6种溶液的pH:
| 溶液 | CH3COONa | Na2CO3 | Na2CO3 | HClO | C6H5ONa |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.3 |
和较强酸的盐,如:2CH3COOH+Na2CO3═2CH3COONa+CO2↑+H2O,若换个角度看,它同时揭示出另一条
规律:碱性较强的物质发生类似反应可以生成碱性较弱的物质.依照该规律,请判断下列反应不能发生的是AD(填编号).
A.CO2+H2O+2NaClO→Na2CO3+2HClO
B.CO2+H2O+NaClO→NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
(2)得根据前述信息判断,常温下,浓度均为0.05mol/L的下列5种物质的溶液中,pH最小的是⑤(填编号),其pH=1(填数值);pH最大的是①(填编号)
①C6H5OH②CH3COOH③HClO4④HClO⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律,下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性的钠溶液;
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体.
请根据上述反应,总结出复分解反应的另一规律:复分解反应能向着生成更难溶物质的方向进行.
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可以观察到的现象是白色固体变为黄色,反应的离子方程式为I-+AgCl=AgI+Cl-.
11.下列叙述正确的是( )
| A. | 凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 反应2A(g)+B(g)═3C(s)+D(g)在一定条件下能自发进行,说明该反应的△H>0 | |
| D. | SO2与SiO2的晶体中,化学键种类和晶体类型均相同 |