题目内容
下列说法中不正确的是
| A.开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B.钢铁是用量最大、用途最广泛的合金 |
| C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| D.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
C
解析试题分析:A.开发使用氢能、太阳能、风能、生物质能等都可以减少煤、石油的开采及利用,可以减少CO2气体的排放。因此是实现“低碳生活”的有效途径。正确。B.我们在生产、生活中使用最多的金属是铁合金,即钢铁。用途最广泛的金属材料也是铁合金。正确。C.硅自然界中以氧化物、硅酸盐的形式存在。错误。D.利用催化设施,在尾气排放管安装一个催化剂转化器,就可以使汽车尾气中CO和NO发生反应转化为N2、CO2等空气的成分,成为无害气体。正确。
考点:考查能量、物质的性质、元素的存在及汽车尾气的治理问题的知识。

下列关于反应热的说法正确的是
| A.当△H<O时,表示该反应为吸热反应 |
B.已知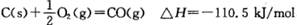 ,说明碳的燃烧热为110kJ/mol ,说明碳的燃烧热为110kJ/mol |
| C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
已知下列热化学方程式:Zn(s) + 1/2 O2(g)= ZnO(s) △H1;Hg(l) + 1/2 O2(g)=HgO(s) △H2;
则 Zn(s)+ HgO(s)=Hg(l)+ ZnO(s),△H值为
| A.△H2-△H1 | B.△H2+△H1 | C.△H1-△H2 | D.-△H1-△H2 |
下列表述不正确的是
| A.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
| B.铝热反应会放出大量的热,因此常温下就能顺利发生 |
| C.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
D.对于化学反应COCl2(g) CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 |
已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ·g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH ="-890" kJ/mol CO2(g)+2H2O(l) ΔH ="-890" kJ/mol |
B.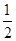 CH4(g)+O2(g) CH4(g)+O2(g) 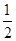 CO2(g)+H2O(l) ΔH="-445" kJ/mol CO2(g)+H2O(l) ΔH="-445" kJ/mol |
C.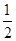 CO2(g)+H2O(l) CO2(g)+H2O(l) 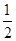 CH4(g)+O2(g) ΔH="+445" kJ/mol CH4(g)+O2(g) ΔH="+445" kJ/mol |
D.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol |
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=-a kJ·mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH=-b kJ·mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(g) ΔH=-c kJ·mol-1(a、b、c均为正数)
对a、b、c三者大小关系的判断正确的是( )
| A.a>b>c | B.a>c>b | C.c>b>a | D.b>a>c |
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)
ΔH=-57.3 kJ/mol下列结论正确的是( )
| A.碳的燃烧热的数值大于110.5 kJ/mol |
| B.①的反应热ΔH为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
下列关于化学反应的描述中正确的是 ( )。
| A.需要加热才能发生的反应一定是吸热反应 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,也放出57.3 kJ的热量 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为2CO(g)+O2(g)=2CO2(g) ΔH=-283.0 kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH=a,2C(s)+O2(g)=2CO(g) ΔH=b,则b>a |
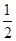 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2