题目内容
1.取四等份铝,分别加入足量的下列溶液中,充分反应后,放出氢气最多的是( )| A. | 3mol/L氨水 | B. | 4mol/L HNO3 | C. | 8mol/L NaOH | D. | 18mol/L H2SO4 |
分析 A、3mol/L氨水与铝不反应;
B、铝与4mol/L HNO3反应不放出氢气,放出NO2等气体;
C、铝与氢氧化钠的水溶液反应生成偏铝酸钠与氢气;
D、铝与浓硫酸发生钝化;
解答 解:A、3mol/L氨水与铝不反应,产生氢气量为0;
B、铝与4mol/L HNO3反应不放出氢气,放出NO2等气体,产生氢气量为0;
C、铝与氢氧化钠的水溶液反应生成偏铝酸钠与氢气;
D、铝与浓硫酸发生钝化,产生氢气量为0;综上所述产生氢气最多的是C,故选C.
点评 本题考查金属铝的性质,较易题,主要考查学生运用所学化学知识综合分析和解决实际问题的能力,该题溶液的浓度不是计算的数据,而是判断溶液属于“浓”或是“稀”,8mol/L以上的HCl、H2SO4、HNO3通常认为是浓酸.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
12.周期表中元素的位置、原子结构与元素的性质之间关系密切.下列说法正确的是( )
| A. | 锗酸(化学式为H4GeO4),是难溶于水的弱酸 | |
| B. | ①硫酸比次氯酸稳定;②S2-易被氯气氧化,均能说明氯元素的非金属性比硫元素强 | |
| C. | 中学教材所附周期表中第15列元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| D. | HF的沸点比HCl 高,是因为H-F键比H-Cl键强 |
13.已知反应2NO(g)+Br2(g)═2NOBr(g)的活化能为a kJ•mol-1,其反应机理如下:
①NO(g)+Br2(g)═NOBr2(g)(慢);
②NO(g)+NOBr2(g)═2NOBr(g)(快)
下列有关该反应的说法正确的是( )
①NO(g)+Br2(g)═NOBr2(g)(慢);
②NO(g)+NOBr2(g)═2NOBr(g)(快)
下列有关该反应的说法正确的是( )
| A. | 反应速率主要取决于②的快慢 | B. | NOBr2是该反应的催化剂 | ||
| C. | 该反应的焓变等于akJ•mol-1 | D. | 反应速率:v(NO)=v(NOBr)=2v(Br2) |
9.在元素周期表短周期元素中,X元素与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20.下列判断正确的是( )
| A. | 四种元素的原子半径:r(Z)>r(X)>r(Y)>r(W) | |
| B. | X、Y、Z、W形成的单质最多有6种 | |
| C. | 四种元素均可与氢元素形成18电子分子 | |
| D. | 四种元素中.Z的最高价氧化物对应水化物酸化最强 |
16. 甲~辛等元素在周期表中的相对物质如下表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的~( )
甲~辛等元素在周期表中的相对物质如下表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的~( )
 甲~辛等元素在周期表中的相对物质如下表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的~( )
甲~辛等元素在周期表中的相对物质如下表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的~( )| A. | 金属性,甲>乙>丁 | |
| B. | 原子半径,辛>戊>甲 | |
| C. | 形成的最简单氢化物的稳定性,己>戊 | |
| D. | 丙与庚的元素原子核外电子数相差13 |
6.化学与生活密切相关,下列说法正确的是( )
| A. | 铝制容器可长期盛放酸性或碱性物质 | |
| B. | 甲烷会导致某些温泉有臭鸡蛋气味 | |
| C. | 太阳能的开发利用可降低碳排放量 | |
| D. | 塑料垃圾会造成水体富营养化 |
13.我国自主研发的生物航空煤油在今年三月首次商业载客飞行成功,该生物航空煤油是以“地沟油”为原料,进行裂化、加氢、去氧处理后得到的.下列说法错误的是( )
| A. | 有机化学中加氢和去氧都属于还原反应 | |
| B. | 裂化是化学变化,裂化产物是饱和烃 | |
| C. | “地沟油”的分子中含有不饱和键,加氢能改善其稳定性 | |
| D. | “地沟油”去氧时,氧主要以H2O和CO2等形式脱去 |
11.生活中处处有化学.下列说法不正确的是( )
| A. | 令人讨厌的地沟油可以用于制肥皂 | |
| B. | 食品中适量添加防腐剂,可以保障安全 | |
| C. | 垃圾分为可回收物、厨余垃圾、有害垃圾、其它垃圾等,废旧电池属于可回收垃圾 | |
| D. | 用红薯酿酒的过程中包含氧化还原反应 |

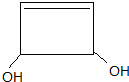 .
.