题目内容
【题目】下列物质中,在一定条件下能发生水解反应,又能发生银镜反应的是
A. 蔗糖B. 葡萄糖
C. 果糖D. 麦芽糖
【答案】D
【解析】
A.蔗糖水解生成葡萄糖和果糖,但不能发生银镜反应;
B.葡萄糖是最简单的糖,不能发生水解,但能发生银镜反应;
C.乙酸乙酯能发生水解生成乙酸和乙醇,但不能发生银镜反应;
D.麦芽糖是二糖,水解只生成葡萄糖,也能发生银镜反应.
A.蔗糖水解的化学方程式为C12H22O11+H2O→C6H12O6(葡萄糖)+C6H12O6(果糖),蔗糖分子结构中无醛基不能发生银镜反应,选项A错误;
B.葡萄糖是最简单的糖,不能发生水解,但葡萄糖在水浴加热条件下发生银镜反应,CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,选项B错误;
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,选项B错误;
C.果糖是最简单的糖,不能发生水解,选项C错误;
D.麦芽糖是二糖,可发生水解化学方程式为C12H22O11+H2O→2C6H12O6(葡萄糖),麦芽糖分子中含有醛基,能发生银镜反应,选项D正确;
答案选D。

【题目】碘及其化合物在生产、生活和科技等方面都有着重要的应用。回答下列问题:
(1)已知:①![]()
②![]()
③![]()
则![]() 与
与![]() 反应生成
反应生成![]() 的热化学方程式为________________________________。
的热化学方程式为________________________________。
(2)反应:![]() 。在716K时,容积均为1L的A、B两个密闭容器中,起始时A容器中充入1mol HI、B容器中充入
。在716K时,容积均为1L的A、B两个密闭容器中,起始时A容器中充入1mol HI、B容器中充入![]() 、
、![]() 各0.5mol,气体混合物中碘化氢的物质的量
各0.5mol,气体混合物中碘化氢的物质的量![]() 与反应时间
与反应时间![]() 的关系如下表:
的关系如下表:
| 0 | 20 | 40 | 60 | 80 | 120 |
A容器 | 1 | 0.91 | 0.85 | 0.81 | 0.795 | 0.784 |
B容器 | 0 | 0.6 | 0.73 | 0.77 | 0.78 | 0.784 |
①120min时,可判断A、B容器反应处于平衡状态,理由是________________。716K时,该反应的平衡常数K=_________________(只列计算式即可)。
②上述反应中,正反应速率为![]() ,逆反应速率为
,逆反应速率为![]() ,其中
,其中![]() 、
、![]() 为速率常数,则
为速率常数,则![]() ________________(以K和
________________(以K和![]() 逆表示)。
逆表示)。
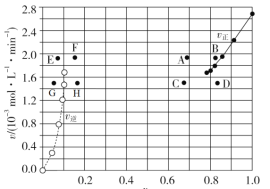
③由A容器中实验数据计算得到![]() 和
和![]() 的关系可用如图表示(
的关系可用如图表示(![]() 为物质的量分数)。当降低到某一温度时,反应重新达到平衡,
为物质的量分数)。当降低到某一温度时,反应重新达到平衡,![]() 和
和![]() 相对应的点可能分别为____、______(填字母)。若向A容器中加入催化剂,则达到平衡时,相对应点的横坐标值______(填“增大”“减小”或“不变”,下同),纵坐标值________。
相对应的点可能分别为____、______(填字母)。若向A容器中加入催化剂,则达到平衡时,相对应点的横坐标值______(填“增大”“减小”或“不变”,下同),纵坐标值________。
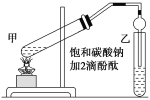
【题目】用图所示装置检验乙烯时不需要除杂的是

乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |