题目内容
【题目】下列说法正确的是( )
A.升高温度能提高活化分子的比例,从而加快反应速率
B.胶体和溶液的本质区别是有无丁达尔效应
C.将![]() 饱和溶液滴入
饱和溶液滴入![]() 溶液中,可获得
溶液中,可获得![]() 胶体
胶体
D.![]() 与
与![]() 都属于酸性氧化物,都能与水反应生成相应的酸
都属于酸性氧化物,都能与水反应生成相应的酸
【答案】A
【解析】
A.升高温度单位体积内活化分子总数增大,活化分子百分含量增大,发生有效碰撞的几率增大,反应速率加快,故A正确;
B.胶体和溶液的本质区别是分散质粒子的直径大小不同,胶体能产生丁达尔效应,溶液不能,可用丁达尔效应区分二者,但丁达尔效应不是本质区别,故B错误;
C.将![]() 饱和溶液滴入
饱和溶液滴入![]() 溶液中,获得
溶液中,获得![]() 沉淀,制备
沉淀,制备![]() 胶体应将饱和
胶体应将饱和![]() 溶液滴加至沸水中至溶液变为红褐色,故C错误;
溶液滴加至沸水中至溶液变为红褐色,故C错误;
D.![]() 与
与![]() 都属于酸性氧化物,二氧化碳能与水反应生成碳酸,二氧化硅不与水反应,故D错误;
都属于酸性氧化物,二氧化碳能与水反应生成碳酸,二氧化硅不与水反应,故D错误;
答案选A。

【题目】近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时发生反应CO(g)+2H2(g) ![]() CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 5 |
n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
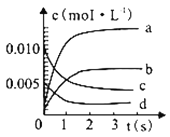
(1)图中表示CH3OH 的变化的曲线是_______;
(2)下列措施不能提高反应速率的有_________(请用相应字母填空);
a 升高温度 b 加入催化剂 c 增大压强 d 及时分离出CH3OH
(3)下列叙述能说明反应达到平衡状态的是__________(请用相应字母填空);
a.CO和H2的浓度保持不变
b.v(H2)=2 v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H键断裂
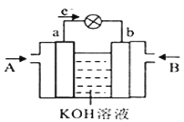
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从__________(填A或B)通入,b极的电极反应式是__________。