题目内容
现有下列各组溶液:
①10℃时10 mL 0.1 mol·L-1的Na2S2O3溶液和50 mL0.05 mol·L-1的H2SO4溶液;
②10℃时10 mL 0.05 mol·L-1的Na2S2O3溶液和10 mL 0.1 mol·L-1的H2SO4溶液;
③30℃时10 mL 0.05 mol·L-1的Na2S2O3溶液和10 mL 0.1 mol·L-1的H2SO4溶液。
若同时将它们混合发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,则出现浑浊的先后顺序是( )
| A.①②③ | B.②①③ | C.③②① | D.①③② |
C
解析

练习册系列答案
相关题目
对于在恒温恒容容器中进行的反应A(g)+2B(g)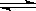 3C(g)+D(g),以下不能说明已达平衡状态的是
3C(g)+D(g),以下不能说明已达平衡状态的是
| A.反应容器中,压强不随时间改变而改变 |
| B.单位时间内生成3nmolC的同时生成nmolA |
| C.反应容器中,混合气体的平均相对分子质量不再改变 |
| D.反应容器中的气体密度不随时间变化 |
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。下列判断正确的是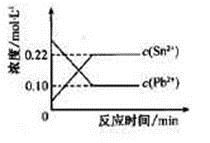
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
一定温度下,反应A2(g)+B2(g)??2AB(g)达到平衡的标志是( )
| A.单位时间内生成n mol A2的同时生成n mol AB |
| B.容器内的总压强不随时间的变化而变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.单位时间内生成n mol A2的同时生成n mol B2 |
下列说法正确的是( )
| A.一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH>0 ΔS>0 |
| B.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
C.常温下,2H2O 2H2↑+O2↑,即常温下水的分解反应是自发反应 2H2↑+O2↑,即常温下水的分解反应是自发反应 |
| D.对于反应H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图(2)所示。
则下列结论正确的是
| A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1 |
B.容器中发生的反应可表示为3X(g)+Y(g)  2Z(g) 2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图(3)所示,则改变的条件是增大压强 |
[双选题]可逆反应2A(g)+B(g) 3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )
3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )
| A.C和D可能都是固体 |
| B.C和D一定都是气体 |
| C.若D为固体,则C一定是气体 |
| D.C和D可能都是气体 |
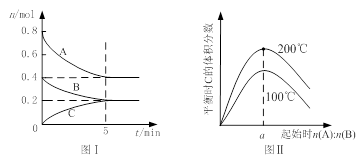
 zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是