题目内容
将15.2gFe、Cu组成的合金溶于过量的稀硝酸中,生成4.48LNO(标准状况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为
| A.33.2g | B.25.4g | C.22.4g | D.19.6g |
B
解析试题分析:由题意和得失电子守恒写出铁、铜与稀硝酸反应生成NO气体的对应关系为Fe~NO,3Cu~2NO,设出铁、铜的物质的量,表示出生成的NO的量,由二者总质量为15.2 g,生成NO0.2mol可以列出方程组进行计算,然后可求得最终生成的氢氧化铁和氢氧化铜的质量为25.4 g。
考点:考查氧化还原反应,考查考生对氧化还原反应及有关计算的掌握。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在一定温度和压强下,1体积X2气体与3体积Y2气体化合生成2体积气体化合物,则该气体化合物的化学式为
| A.X2Y3 | B.XY3 | C.XY | D.X3Y |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol的2H35Cl含中子数为1.8NA |
| B.16g O3和O2混合物中氧原子数为NA |
| C.常温下,1L pH=l的溶液中H+的数目大于0.1NA |
| D.0.1 mol的H2O2中含有非极性键数为0.2NA |
下列有关化学用语表示正确的是
A.S2-的结构示意图: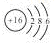 |
| B.常用于考古中文献年代确定的原子:14 6C |
C.H2CO3的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| D.4g H2在空气25℃.101kPa下燃烧,生成液态的水放出571.6kJ·mol-1的热量,则该反应的热化学方程式为:2H2(g)+O2(g)==2H2O(g);△H=-571.6kJ/mol |
一定质量的某铁的氧化物FexOy,与足量4 mol/L稀硝酸溶液充分反应,消耗硝酸700mL,放出2.24LNO气体(标准状况)。则该铁的氧化物的化学式为
| A.FeO | B.Fe2O3 | C.Fe3O4 | D.Fe8O10 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.0.5 L 1 mol/L NaHS溶液中,N(Na+)+N(HS—)=NA |
| B.12.4 g白磷(分子式为P4)中含有P—P共价键0.6 NA |
| C.常温下,pH=2的醋酸溶液中所含有的H+数为0.01 NA |
| D.将92 g N2O4晶体放入容器中,恢复到常温常压时,所含气体分子数为NA |
0.001mol金属放入10mL0.1mol/L某酸溶液中,产生22.4mL氢气(标准状况),下列情况中一定不可能的是
| A.一价金属和一元酸 | B.二价金属和二元酸 |
| C.三价金属和二元酸 | D.二价金属和一元酸 |
20g由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2L氢气(标准状况),这种金属混合物的组成可能是
| A.Mg和Al | B.Al和Fe |
| C.Fe和Zn | D.Zn和Cu |