题目内容
下列有关化学用语表示正确的是
A.S2-的结构示意图: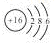 |
| B.常用于考古中文献年代确定的原子:14 6C |
C.H2CO3的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| D.4g H2在空气25℃.101kPa下燃烧,生成液态的水放出571.6kJ·mol-1的热量,则该反应的热化学方程式为:2H2(g)+O2(g)==2H2O(g);△H=-571.6kJ/mol |
B
解析试题分析: A、S2-的最外层有18个e-,错误;B、14 6C常用于考古中文献年代确定,正确;C、H2CO3的电离分两步进行,不能并成一步书写,错误;D、提供的数据是生成液态水时的数据,而热化学方程式中水为气态,错误。
考点:考查化学用语、电离方程式、热化学方程式。

练习册系列答案
相关题目
有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为
| A.(y-2x)/a, | B.(y-x)/a, | C.(2y-2x)/a, | D.(2y-4x)/a。 |
用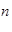 A表示阿伏加德罗常数的值。下列说法正确的是
A表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol Cl-离子中含有的电子数为8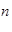 A A |
B.标准状况下,2.24 L H20中含有的分子数为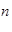 A A |
C.27g铝与足量的氧气反应,转移的电子数为3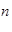 A A |
D.0.2 mo1·L-1 Ca(NO3)2溶液中含有的N03-离子数为0.4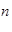 A A |
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.25℃时,pH=1的1.0 LH2SO4溶液中含有的H+的数目为0.2NA |
| B.标准状况下,2.24 LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.取0.5 L 0.2 mol·L-1mol氯化铁溶液 ,所得溶液含有0.1 NA个Fe3+ |
NO、NO2、O2按照一定比例通入水中,能被完全吸收,无剩余气体,若NO、NO2、O2的气体体积分别为a、b、 c、则a:b:c可能为( )
| A.1:5:2 | B.2:5:1 | C.5:1:2 | D.5:2:1 |
将15.2gFe、Cu组成的合金溶于过量的稀硝酸中,生成4.48LNO(标准状况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为
| A.33.2g | B.25.4g | C.22.4g | D.19.6g |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.24g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
| C.在碳酸钠溶液中,若c(CO32-)="1" mol?L-1,则c(Na+)="2" mol?L-1 |
| D.通过MnO2催化使H2O2分解,产生32gO2时转移电子数为2NA |
设阿伏加德罗常数的值为NA,下列说法正确的是
| A.在常温常压下,11.2LN2含有的分子数为0.5NA |
| B.在常温常压下,1molH2含有的原子数为2NA |
| C.0.1mol/LNaCl溶液中含有Na+数目为0.1NA |
| D.在同温同压时,相同体积的任何气体含有相同数目的原子 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,33.6L氟气中含有氟原子的数目为1.5NA |
| B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| C.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
| D.50mL18.4mol·L-1浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA |