题目内容
13.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为物质系数.在2s内,用X表示平均速率为0.3m/p mol/(L•s),则在2s内,Q物质增加的物质的量为( )| A. | 1.2q/p mol | B. | 1.2m/p mol | C. | 0.6q/p mol | D. | 0.3q/p mol |
分析 由反应速率之比等于化学计量数比计算v(Q),然后根据△Q=v(Q)×V×△t计算Q物质增加的物质的量.
解答 解:在2s内,用X表示平均速率为0.3m/p mol/(L•s),由反应速率之比等于化学计量数比,可以得出用Q表示平均速率为0.3m/p mol/(L•s)×$\frac{q}{m}$=$\frac{0.3q}{p}$mol/(L•s),
则2s内,Q物质增加的物质的量是$\frac{0.3q}{p}$mol/(L•s)×2L×2s=$\frac{1.2q}{p}$mol,
故选A.
点评 本题考查化学反应速率的表示方法和计算,难度吧.注意反应速率之比等于化学计量数比、及速率表达式的变形灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式: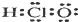 | B. | 氯化钠的分子式:NaCl | ||
| C. | 二氧化碳的比例模型: | D. | Cl-的结构示意图: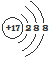 |
8.下列反应中,水作还原剂的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 3NO2+H2O═2HNO3+NO | D. | 2F2+2H2O═4HF+O2 |
5.如图所示,锥形瓶内有气体X,分液漏斗内有液体Y,如果Y流下,过一会儿,小气球鼓起,气体X和Y不可能是( )
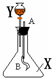

| A. | X是NH3,Y是KCl溶液 | B. | X是SO2,Y是NaOH | ||
| C. | X是H2,Y是浓硫酸 | D. | X是CO2,Y是KOH |
2.电解法炼铝时,冰晶石的作用是( )
| A. | 助熔剂 | B. | 催化剂 | C. | 还原剂 | D. | 氧化剂 |