题目内容
6.下列物质中存在的化学键,在熔化时没有破坏的是( )| A. | 金属铜 | B. | 碘 | C. | 固体氮 | D. | 硫酸钠 |
分析 物质熔化时,离子晶体、原子晶体和金属晶体化学键收到破坏,分子晶体化学键不被破坏,据此解答.
解答 解:金属铜为金属晶体,熔化时,金属键被破坏;硫酸钠为离子晶体,熔化时,离子键被破坏;碘、固体氮为分子晶体,熔化时不破坏化学键,只破坏分子间作用力,
故选:BC.
点评 本题考查了化学键,明确晶体的构成微粒及微粒之间存在的作用力即可解答,题目难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
16.下列反应的离子方程式书写正确的是( )
| A. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| D. | NaHSO4溶液中加入Ba(OH)2溶液后恰好显中性Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
1.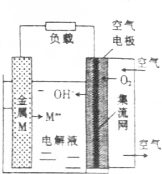 2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )
2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )
 2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )
2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )| A. | 电池工作时,电子沿金属M→负载→空气电极流动 | |
| B. | 若M为Al,电解液为NaC1溶液.则电池工作一段时间后.电解液的pH增大 | |
| C. | 若M为Mg.电解液为NaCl溶液,则电池的总反应方程式为2Mg+O2+2H2O═2Mg(OH)2 | |
| D. | 集流网可增大接触面,从而吸附更多的氧气,提高金属电池的工作效率. |
20.某溶液有Cl-、CO32-、SO42-,要求依次检验出这三种离子,请完成下列设计:
| 检验离子 | 所加试剂 | 实验现象 | 离子方程式 |
| ①CO32- | 有气泡产生 | ||
| ②SO42- | 产生白色沉淀 | ||
| ③Cl- | 产生白色沉淀 |

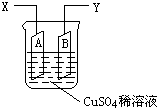 如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100mLCuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y.
如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100mLCuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y.