题目内容
16.已知酸性:H2SO4>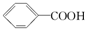 >H2CO3>
>H2CO3>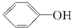 >HCO3-,综合考虑反应物的转化率和原料成本等因素,将
>HCO3-,综合考虑反应物的转化率和原料成本等因素,将 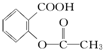 转变为
转变为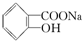 的最佳方法是( )
的最佳方法是( )| A. | 与足量的NaOH溶液共热后,再通入足量CO2 | |
| B. | 与足量的NaOH溶液共热后,再加入适量H2SO4 | |
| C. | 与稀H2SO4共热后,加入足量的NaOH溶液 | |
| D. | 与稀H2SO4共热后,加入足量的Na2CO3溶液 |
分析  在碱性条件下水解生成
在碱性条件下水解生成 ,酸性:苯甲酸>碳酸>苯酚,只要向
,酸性:苯甲酸>碳酸>苯酚,只要向 溶液中通入过量二氧化碳即可实现,据此分析解答.
溶液中通入过量二氧化碳即可实现,据此分析解答.
解答 解:A、碱性条件下, 水解生成
水解生成 ,然后通入过量二氧化碳生成
,然后通入过量二氧化碳生成
B、碱性条件下, 水解生成
水解生成 ,然后加入稀硫酸生成
,然后加入稀硫酸生成 ,而得不到
,而得不到
C、酸性条件下, 水解生成
水解生成 ,然后加入NaOH溶液时生成
,然后加入NaOH溶液时生成 而得不到
而得不到
D、 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量Na2CO3溶液生成
,再加入足量Na2CO3溶液生成 ,得不到
,得不到 ,故D错误,故选A.
,故D错误,故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸性质的考查,注意酸性的比较及应用,题目难度不大.

练习册系列答案
相关题目
6. 25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
 25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )| A. | 当c(HS-)>c(S2-)时,溶液一定显酸性 | |
| B. | 当pH=7时,溶液中有c(Na+)=c(HS-)+2c(S2-)+c(H2S) | |
| C. | 当4<pH时,向其中滴加0.1mol/LCuSO4都有CuS沉淀(Ksp(CuS)=6.3×10-36) | |
| D. | 当pH=9时,溶液中有c(H+)=c(OH-)+c(HS-) |
4.下列离子或分子在溶液中能大量共存的是( )
| A. | K+.Al3+.Cl-.NO3- | B. | K+.Fe3+.Cl-.SiO32- | ||
| C. | H+.Fe2+.SO42-.Br2 | D. | K+.Ag+.NH3•H2O.NO3- |
11.Al(OH)3即能与酸起反应,又能与强碱溶液起反应生成盐和水,说明Al(OH)3属于( )
| A. | 两性氧化物 | B. | 两性氢氧化物 | C. | 盐 | D. | 有机物 |
8.国际无机化学命名委员会在1989年做出决定,把元素周期表原先的主、副族及族号取消,由左至右改为18列.如碱金属元素为第1列,稀有气体元素为第18列.按此规定,下列说法错误的是( )
| A. | 只有第2列元素的原子最外层有2个电子 | |
| B. | 第3列元素种类最多 | |
| C. | 第15列元素的最高价氧化物为R2O5 | |
| D. | 第17列元素的第一种元素无含氧酸 |
5.Co(Ⅲ)的八面体配合物CoClm•nNH3,若1mol 配合物与足量AgNO3溶液作用生成1mol AgCl沉淀,则m、n的值是( )
| A. | m=1,n=5 | B. | m=3,n=4 | C. | m=5,n=1 | D. | m=3,n=3 |
6.下列说法中,正确的是 ( )
| A. | 构成分子晶体的微粒中一定含有共价键 | |
| B. | 在结构相似的情况下,原子晶体中的共价键越强,晶体的熔沸点越高 | |
| C. | 某分子晶体的熔、沸点越高,分子晶体中共价键的键能越大 | |
| D. | 分子晶体中只存在分子间作用力而不存在任何化学键,所以其熔、沸点一般较低 |
 有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30).A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2.则:
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30).A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2.则: