题目内容
向两份a mL b mol/L的稀盐酸中分别加入x mL的水和y mL b mol/L Ba(OH)2溶液,此时两溶液的pH恰好相等,则x、y的关系符合(式中a、b均大于零,设两溶液混合时的体积有加和性)( )
| A、y=2ax+b | ||||
B、y=
| ||||
C、
| ||||
D、x=
|
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:向两份a mL b mol/L的稀盐酸中分别加入x mL的水和y mL b mol/L Ba(OH)2溶液,此时两溶液的pH恰好相等,说明溶液显示酸性,混合后的溶液中氢离子浓度相等,然后根据稀盐酸的稀释、酸碱中和反应计算出溶液中氢离子浓度,两混合液中氢离子浓度一定相等,据此进行解答.
解答:
解:a mL b mol/L的稀盐酸中加入x mL的水,溶液中氢离子浓度为:c(H+)=
=
mol/L,
a mL b mol/L的稀盐酸中加入y mL b mol/L Ba(OH)2溶液,反应后的溶液中氢离子浓度为:
=
mol/L,
混合液的pH恰好相等,则氢离子浓度相等,即:
mol/L=
mol/L,
整理可得:y=
,该该关系变形可得:
-
=1,
故选BC.
| bmol/L×a×10-3L |
| (a+x)×10-3L |
| ab |
| a+x |
a mL b mol/L的稀盐酸中加入y mL b mol/L Ba(OH)2溶液,反应后的溶液中氢离子浓度为:
| bmol/L×a×10-3L-2×bmol/L×y×10-3L |
| (a+y)×10-3L |
| ab-2by |
| a+y |
混合液的pH恰好相等,则氢离子浓度相等,即:
| ab |
| a+x |
| ab-2by |
| a+y |
整理可得:y=
| ax |
| (2x+3a) |
| a |
| 2y |
| 3a |
| 2x |
故选BC.
点评:本题考查了溶液的稀释、酸碱中和反应的计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确两混合液中氢离子浓度相等为解答本题的关键,注意氢氧化钡中氢氧根离子的数目.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
以下物质检验的方法、现象和结论,其中错误的是( )
| A、某盐溶液中加入氯水,再加入KSCN溶液,溶液出现血红色,则原溶液中含有Fe2+ |
| B、某盐加入浓的氢氧化钠溶液并加热,能产生使润湿的红色石蕊试纸变蓝的气体,则该盐是铵盐 |
| C、常温下氯酸钾和浓盐酸反应所产生的气体用湿润的淀粉碘化钾试纸检验变蓝,该气体是Cl2 |
| D、用洁净的铂丝蘸取该溶液,置于火焰上灼烧,能观察到火焰呈黄色.该溶液中一定含有钠离子,可能含有钾离子 |
按微粒的半径从大到小的顺序排列的是( )
| A、Mg、Al、Na |
| B、Li、Na、K |
| C、Cl、S、P |
| D、N、O、F |
化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质.这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的( )

| A、常温下,化合物A、B、C、D均为气体 |
| B、如图所示的五个转化关系中,有三个是化合反应 |
| C、如图所示的五个转化关系中,均为氧化还原反应 |
| D、上述转化关系所涉及的化合物中只有一种是电解质 |
韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”.则关于“暖冰”的判断正确的是( )
| A、“暖冰”中存在离子键 |
| B、“暖冰”中水分子的O-H键是非极性键 |
| C、“暖冰”的密度大,有导电性和导热性 |
| D、水凝固形成20℃时的“暖冰”所发生的变化是物理变化 |
下列离子方程式中不正确的是( )
| A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| C、氢氧化钠和少量氢硫酸反应:2OH-+H2S=S2-+2H2O |
| D、在澄清石灰水中通入过量二氧化碳:OH-+CO2=HCO3- |
微粒甲与微粒乙在溶液中的转化关系如图所示: ,微粒甲不可能是( )
,微粒甲不可能是( )
 ,微粒甲不可能是( )
,微粒甲不可能是( )| A、CO2 |
| B、NH4+ |
| C、Al3+ |
| D、SiO2 |
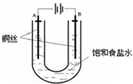 已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )
已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )| A、B极发生的电极反应为2H++2e-=H2↑ |
| B、实验开始时,A极附近出现白色浑浊 |
| C、电解时,Na+移向A极 |
| D、一段时间后,U形管底部形成橙黄色沉淀 |
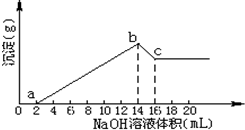 将一定质量的Mg,Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得如图关系.
将一定质量的Mg,Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得如图关系.