题目内容
7.已知25℃时,Ksp(CaSO4)=7.10×10-5.在0.100L 0.200mol•L-1CaCl2溶液中加入2.72g CaSO4粉末充分搅拌后,假设溶液的体积变化忽略不计,则溶液中SO42-物质的量浓度为:3.55×10-4mol•L-1.分析 据c(SO42-)=$\frac{Ksp}{c(C{a}^{2+})}$和钙离子浓度计算.
解答 解:c(SO42-)=$\frac{Ksp}{c(C{a}^{2+})}$=$\frac{7.1×1{0}^{-5}}{0.2}$=3.55×10-4 mol/L,故答案为:3.55×10-4.
点评 本题考查了关于沉淀的溶度积的计算,题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
18.在下列影响化学反应速率因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末.
| A. | 只有①②③ | B. | 只有①②④ | C. | 只有③④ | D. | ①②③④ |
15.对如表实验现象或操作解释错误的是( )
| 现象或操作 | 解 释 | |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 |
| B | 配制SnCl2溶液时,先将SnCl2溶于适量稀盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的锡粒 | 抑制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 不能说明该溶液中一定含有SO42- |
| D | 向浓度均为0.1mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,首先生成蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
2.下列各组有机物中,只需加入溴水就能一 一鉴别的是( )
| A. | 甲苯、苯、己烯 | B. | 己炔、己烯、四氯化碳 | ||
| C. | 己烯、苯、乙醇 | D. | 己烯、苯、煤油 |
3.已知浓硫酸与木炭粉在加热条件下的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑十CO2↑2H2O↑.酸性KMnO4溶液可以吸收SO2,试用如图所示各装置设计一个实验,验证上述反应所产生的各种产物.
(1)这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):④→②→①→③.
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
| 编号 | ① | ② | ③ | ④ |
| 装置 | 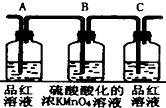 | 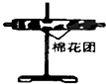 |  | 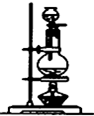 |
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
20.下列物质的分类采用树状分类法的是( )
| A. | 铁是单质,又是导体 | |
| B. | 氧化物可分为金属氧化物和非金属氧化物 | |
| C. | 氯化钠是钠的化合物,又是氯化物 | |
| D. | 氢氧化钙是纯净物、化合物,又是碱 |