题目内容
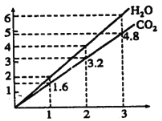
【题目】在一密闭容器中通入A、B、C三种气体,保持一定温度,在t1~t4s时测得各物质的浓度如表,则下列判断正确的是
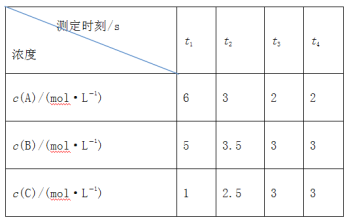
A.在t3s时反应已经停止
B.t3~t4s内正、逆反应速率不相等
C.在容器中发生的反应为A(g)+B(g)![]() C(g)
C(g)
D.在t2~t3s内A的平均反应速率为![]() mol·L1·s1
mol·L1·s1
【答案】D
【解析】
A.由题给数据可知,t3 s时可逆反应达到化学平衡状态,此时v(正)=v(逆)≠0,反应并未停止,故A错误;
B.t3~t4 s内,A、B、C的浓度没有发生变化,反应处于化学平衡状态,正、逆反应速率相等,故B错误;
C.达到化学平衡状态时,A、B、C的浓度变化量之比为(6-2)∶(5-3)∶(3-1)=2∶1∶1,故该反应的化学方程式为2A(g)+B(g)![]() C(g),故C错误;
C(g),故C错误;
D.t2~t3 s内,Δc(A)=1 mol·L1,故用A表示的该时间段的平均化学反应速率为![]() mol·L1·s1,故D正确;
mol·L1·s1,故D正确;
故答案选D。

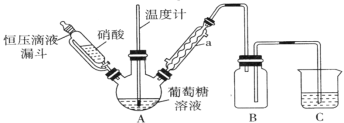
【题目】实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH![]() CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):
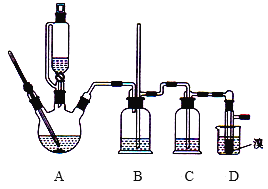
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点/(℃) | 78.5 | 132 | 34.6 |
熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:______。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是______。
(4)在装置C中应加入____ (填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层。
(6)若产物中有少量副产物乙醚,可用____的方法除去。