题目内容
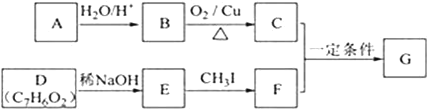
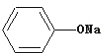
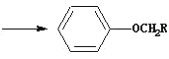
【题目】有机物M的结构简式如图,有关M的下列叙述中正确的是

A. 可与H2反应,1 molM最多消耗1 molH2
B. 可与浓溴水反应,1molM最多消耗4 molBr2
C. 可与NaOH溶液反应,1 mol M最多消耗3 molNaOH
D. 常温下,M在水中的溶解度小于苯酚在水中的溶解度
【答案】D
【解析】
A.能与氢气发生加成反应的有苯环和碳碳双键,则1molM最多消耗4molH2,故A错误;
B.能与溴水发生反应有酚羟基的邻位H原子以及碳碳双键与溴水的加成反应,1molM最多消耗3molBr2,故B错误;
C.有机物M水解产物含有2个酚羟基、1个羧基、羟基和HCl,其中能与NaOH反应的为酚羟基、羧基和HCl,与NaOH溶液反应,1molM最多消耗4molNaOH,故C错误;
D.有机物M含有酯基,为憎水基,M在水中的溶解度小于苯酚在水中的溶解度,故D正确;
故答案为D。

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
试回答下列问题:
(1)元素E在元素周期表中的位置是______。
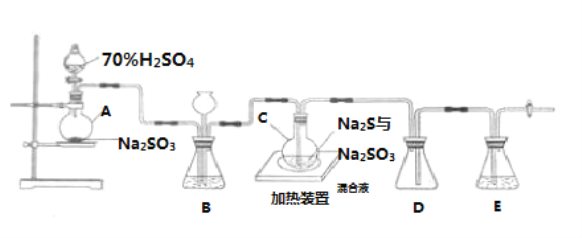
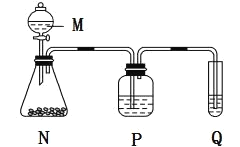
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____,Q中观察到的实验现象是_____。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有_____。
②b与c反应的化学方程式为_____。
【题目】NiOOH难溶于水,常作电池的正极材料。利用某含镍废料(主要成分为NiO,另含有SiO2、Fe2O3、CuO三种杂质)制备NiOOH的工业流程如图。
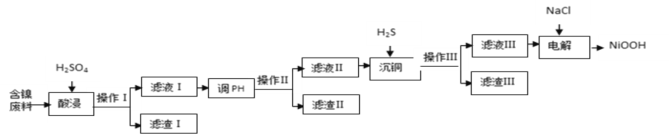
已知:
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | |
开始沉淀的pH | 1.5 | 4.4 | 6.7 |
沉淀完全的pH | 3.7 | 6.9 | 9.2 |
(1)提高酸浸速度的方法为_______________________、_____________________(任写2条)
(2)滤渣Ⅰ的成分为__________;若滤渣Ⅱ为Fe(OH)3,则“调pH”的范围为_____________.
(3)沉铜时发生反应的离子方程式为______________________________________________。
(4)电解过程是控制在碱性条件下阳极产生ClO-,并用ClO-将Ni2+氧化的过程。请写出氧化过程中发生反应的离子方程式____________________________________________________。