题目内容
分类是常用的学习方法,对于反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑的分类错误的是
| A.化合反应 | B.氧化还原反应 | C.离子反应 | D.放热反应 |
A
解析试题分析:化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;据此进行分析判断2Al+2NaOH+2H2O=2NaAlO2+3H2↑不是化合反应。所以选A。
考点:考查物质的分类。

 金钥匙试卷系列答案
金钥匙试卷系列答案在化学反应中,某元素由化合态变为单质,则该元素
| A.一定被氧化 | B.一定被还原 |
| C.既可能被氧化,也可能被还原 | D.以上都不是 |
将一定质量铜与100 mL一定浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液加入140 mL 5 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度是
| A.5 mol/L | B.7 mol/L | C.10 mol/L | D.12 mol/L |
现有含0.1 mol/L的SO32-溶液30 mL,恰好被2×10-3 mol XO4-氧化为SO42-,则元素X在还原产物中的化合价是
| A.+4 | B.+3 | C.+2 | D.+1 |
下列反应属于氧化还原反应,但水既没有做氧化剂又没有做还原剂的是
| A.2F2+2H2O ="4HF" +O2 |
| B.3NO2+H2O =2HNO3+NO |
| C.2Na +2H2O=2NaOH+H2 |
| D.CaO+H2O =Ca(OH)2 |
代硫酸钠可用作脱氯剂,已知25.0 mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下112 mL Cl2完全转化为Cl-时,S2O32-转化成( )
| A.S2- | B.S | C.SO32- | D.SO42- |
将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
| A.6.72 L | B.11.2 L | C.22.4 L | D.4.48 L |
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,
则下列有关说法中不正确的是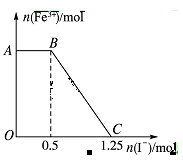
| A.图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D.向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
在一种酸性溶液中,可能存在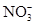 、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
| A.一定有碘离子 | B.可能含铁离子 |
| C.可能有氯离子 | D.不含硝酸根离子 |