题目内容
将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
| A.6.72 L | B.11.2 L | C.22.4 L | D.4.48 L |
A
解析试题分析:合金溶于足量的NaOH溶液中,金属铝和氢氧化钠反应产生气体氢气3.36L(标准状况)物质的量为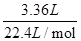 =0.15mol,根据电子转移守恒可知n(Al)=
=0.15mol,根据电子转移守恒可知n(Al)=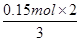 =0.1mol,故金属铝的质量为0.1mol×27g/mol=2.7g,金属铝提供电子的量是0.3mol。由题意可知,向反应后的溶液中加入过量NaOH溶液后,铝离子全部转化为偏铝酸根离子,不会出现沉淀,反应后产生19.4g氢氧化镁、氢氧化铁沉淀的,沉淀中氢氧根的质量为19.4g-(11.9g-2.7g)=10.2g,物质的量n(OH-)=
=0.1mol,故金属铝的质量为0.1mol×27g/mol=2.7g,金属铝提供电子的量是0.3mol。由题意可知,向反应后的溶液中加入过量NaOH溶液后,铝离子全部转化为偏铝酸根离子,不会出现沉淀,反应后产生19.4g氢氧化镁、氢氧化铁沉淀的,沉淀中氢氧根的质量为19.4g-(11.9g-2.7g)=10.2g,物质的量n(OH-)=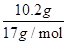 =0.6mol。反应中金属铁、铜提供的电子的物质的量等于生成碱的氢氧根离子的物质的量即0.6mol。将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共提供电子的物质的量为0.6+0.3=0.9mol,令NO的物质的量为xmol,根据电子转移守恒有(5-2)×xmol=0.9mol,解得x=0.3,所以生成的NO的体积为0.3mol×22.4L/mol=6.72L,故A正确。
=0.6mol。反应中金属铁、铜提供的电子的物质的量等于生成碱的氢氧根离子的物质的量即0.6mol。将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共提供电子的物质的量为0.6+0.3=0.9mol,令NO的物质的量为xmol,根据电子转移守恒有(5-2)×xmol=0.9mol,解得x=0.3,所以生成的NO的体积为0.3mol×22.4L/mol=6.72L,故A正确。
考点:混合物反应的有关计算;化学反应方程式的有关计算

 阅读快车系列答案
阅读快车系列答案属于非氧化还原反应的是
| A.分解反应 | B.复分解反应 | C.吸热反应 | D.银镜反应 |
分类是常用的学习方法,对于反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑的分类错误的是
| A.化合反应 | B.氧化还原反应 | C.离子反应 | D.放热反应 |
下列化合物中氮元素只具有还原性的是
| A.KNO3 | B.HNO3 | C.NO | D.NH3 |
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于区域3的是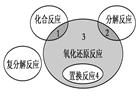
| A.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
B.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
C.4NH3+5O2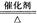 4NO+6H2O 4NO+6H2O |
| D.Fe+CuSO4=FeSO4+Cu |
下列属于右边关系图中阴影部分的化学反应是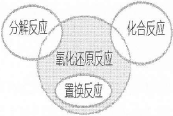
A.2Na+O2 Na2O2 Na2O2 |
| B.2Na2O2+2CO2=2Na2CO3+O2 |
C.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| D.Fe+H2SO4=FeSO4+H2↑ |
宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”涉及的化学反应是 4Ag+2H2S+O2→2X+2H2O,下列说法正确的是
| A.X的化学式为AgS |
| B.银针验毒时,空气中氧气失去电子 |
| C.反应中Ag和H2S均是还原剂 |
| D.每生成1mo1X,反应转移2mo1电子 |
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性溶液中可以产生Cl2,下列关于混盐CaOCl2的有关判断不正确的是(NA为阿伏加德罗常数)
| A.该混盐在酸性溶液中产生1mol Cl2时转移的电子数为NA |
| B.该混盐的水溶液显碱性 |
| C.该混盐中氯元素的化合价为+1和-1价 |
| D.该混盐具有较强的还原性 |
下列有关氧化还原反应的叙述中,正确的是
| A.一定有氧气参加 | B.还原剂本身被还原 |
| C.氧化反应先于还原反应发生 | D.一定有电子转移(得失或偏移) |