题目内容
在一种酸性溶液中,可能存在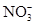 、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
| A.一定有碘离子 | B.可能含铁离子 |
| C.可能有氯离子 | D.不含硝酸根离子 |
B
解析

练习册系列答案
相关题目
1.92 g Cu投入到一定量的浓硝酸中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 ml气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为
| A.504 ml | B.336 ml | C.224 ml | D.168 ml |
属于非氧化还原反应的是
| A.分解反应 | B.复分解反应 | C.吸热反应 | D.银镜反应 |
分类是常用的学习方法,对于反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑的分类错误的是
| A.化合反应 | B.氧化还原反应 | C.离子反应 | D.放热反应 |
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2 +O2↑。下列对此反应的说法中,不正确的是( )
+O2↑。下列对此反应的说法中,不正确的是( )
| A.方框中的物质为Na2SO4 |
| B.Na2O2既是氧化剂,又是还原剂 |
| C.Na2FeO4既是氧化产物,又是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共转移8 mol电子 |
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125 ℃分解为LiH、H2和Al。下列叙述错误的是( )。
| A.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
| B.LiAlH4与D2O反应,所得氢气的摩尔质量为4 g·mol-1 |
| C.1 mol LiAlH4在125 ℃完全分解,转移3 mol电子 |
| D.LiAlH4与水反应生成三种物质时,化学方程式可表示为:LiAlH4+4H2O=Al(OH)3+LiOH+4H2↑ |
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B.用石膏粉制作石膏雕像 |
| C.用铝质或铁质容器盛放浓硝酸 |
| D.酸雨的形成 |
2011年11月,“神舟八号”在酒泉发射升空,并取得圆满成功。“神舟八号”的运载火箭所用燃料是偏二甲肼(C2H8N2)和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应: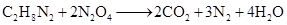 提供能量。下列有关叙述正确的是( )
提供能量。下列有关叙述正确的是( )
| A.该燃料绿色环保,在燃烧过程中不会造成任何环境污染 |
| B.该反应中N2O4是氧化剂,偏二甲肼是还原剂 |
| C.N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物 |
| D.每有0.6 mol N2生成,转移电子数目为2.4NA |
氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有关说法不正确的是 ( )。
| A.由反应可确定氧化性:HClO3>O2 |
| B.由非金属性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合气体的质量为45 g,则反应的化学方程式可表示为3HClO3===2O2↑+Cl2↑+HClO4+H2O |
| D.若化学计量数a=8,b=3,则生成3 mol O2时该反应转移20 mol电子 |