题目内容
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=______,该条件下的平衡常数K=________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”“逆向”或“不”);最终达平衡时NO的转化率a=______________。
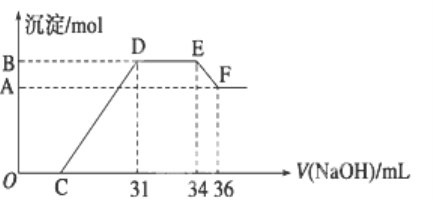
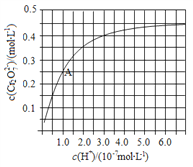
(3)在25 ℃下,向浓度均0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_____沉淀(填化学式),当两种沉淀共存时,溶液中c(Mg2+)/c(Cu2+)=__________(已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)。
【答案】)2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H=﹣747kJ/mol ad0.042mol·L-1·min-1
N2(g)+2CO2(g) △H=﹣747kJ/mol ad0.042mol·L-1·min-1![]() >正向60%Cu(OH)28.2×108或
>正向60%Cu(OH)28.2×108或![]() ×109
×109
【解析】
(1)根据平衡常数的定义,若平衡常数表达式为K= K=![]() ,则化学方程式为:2CO(g)+2NO(g)
,则化学方程式为:2CO(g)+2NO(g)![]() N2(g)+2CO2(g),已知①2C(s)+O2(g)=2CO(g) ΔH=﹣221 kJ/mol,②C(s)+O2(g)=CO2(g) △H=﹣393.5 kJ/mol,③N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
N2(g)+2CO2(g),已知①2C(s)+O2(g)=2CO(g) ΔH=﹣221 kJ/mol,②C(s)+O2(g)=CO2(g) △H=﹣393.5 kJ/mol,③N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
根据盖斯定律:②×2-①-③得:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H=﹣747 kJ/mol; 由于该反应是气体体积减小的放热反应a.增大容器压强平衡正向移动,NO转化率增大,a正确;b.升高温度平衡逆向移动,NO转化率减小,b错误;c.使用优质催化剂不改变平衡,c错误;d.增大CO的浓度,可以提高NO的转化率,d正确;因此本题答案为:ad。(2)根据盖斯定律:上述已知反应②-③得:C(S)+2NO(g)
N2(g)+2CO2(g) △H=﹣747 kJ/mol; 由于该反应是气体体积减小的放热反应a.增大容器压强平衡正向移动,NO转化率增大,a正确;b.升高温度平衡逆向移动,NO转化率减小,b错误;c.使用优质催化剂不改变平衡,c错误;d.增大CO的浓度,可以提高NO的转化率,d正确;因此本题答案为:ad。(2)根据盖斯定律:上述已知反应②-③得:C(S)+2NO(g)![]() N2(g)+CO2(g) △H=﹣574.5 kJ/mol;①利用表格数据:0~5min内,以N2表示的该反应速v(N2)=
N2(g)+CO2(g) △H=﹣574.5 kJ/mol;①利用表格数据:0~5min内,以N2表示的该反应速v(N2)=![]() =0.042mol·L-1·min-1,所以以CO2表示的该反应速率v(CO2)= v(N2) =0.042mol·L-1·min-1;通过分析知10min后浓度不再改变,处于平衡状态,用三行式分析浓度改变
=0.042mol·L-1·min-1,所以以CO2表示的该反应速率v(CO2)= v(N2) =0.042mol·L-1·min-1;通过分析知10min后浓度不再改变,处于平衡状态,用三行式分析浓度改变
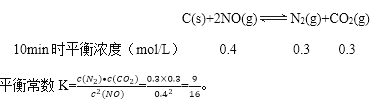
②第15 min后,温度调整到T2,从表格查得NO减少,N2增加,平衡正向移动,由于正反应为放热反应,改变条件为降温,则T1 >T2。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,此时各量分析如下:
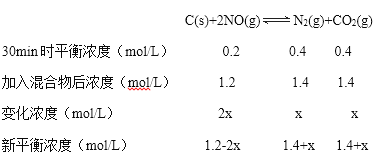
T2时平衡常数K=![]() =4, 加入混合物后Qc=
=4, 加入混合物后Qc=![]() =1.36<K,则此时反应正向移动;由于温度不变,平衡常数为定值,新平衡时有:
=1.36<K,则此时反应正向移动;由于温度不变,平衡常数为定值,新平衡时有:![]() =4,解得x=0.2;经计算NO起始总量为2mol+2mol=4mol,达到新平衡时NO的物质的量为(1.2-2×0.2)mol/L×2L=1.6mol,转化的NO共4mol-1.6mol=2.4mol,所以最终达平衡时NO的转化率a=
=4,解得x=0.2;经计算NO起始总量为2mol+2mol=4mol,达到新平衡时NO的物质的量为(1.2-2×0.2)mol/L×2L=1.6mol,转化的NO共4mol-1.6mol=2.4mol,所以最终达平衡时NO的转化率a=![]() 。(3)由于Ksp[Cu(OH)2]<Ksp[Mg(OH)2],所以先生成Cu(OH)2沉淀;当两种沉淀共存时,溶液是Cu(OH)2、Mg(OH)2的饱和溶液,溶液中OH-离子浓度相同,根据溶度积常数计算,溶液中c(Mg2+)/c(Cu2+)=
。(3)由于Ksp[Cu(OH)2]<Ksp[Mg(OH)2],所以先生成Cu(OH)2沉淀;当两种沉淀共存时,溶液是Cu(OH)2、Mg(OH)2的饱和溶液,溶液中OH-离子浓度相同,根据溶度积常数计算,溶液中c(Mg2+)/c(Cu2+)=![]() =
=![]() =8.2×108,故答案为:8.2×108 或
=8.2×108,故答案为:8.2×108 或![]() ×109。
×109。

【题目】SO2是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也可用作熏蒸剂、防腐剂、消毒剂、还原剂等。
(1)SO2性质多变,若将SO2气体通入氢硫酸中,能看到的现象为:__________,该反应中SO2表现出______性;若将SO2气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中SO2表现出__________性。
(2)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2CaSO4·2H2O碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
余石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。