题目内容
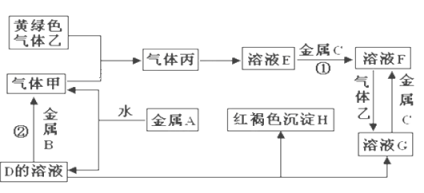
【题目】硅是信息技术的关键材料,在工业中可利用镁制取硅:2Mg(过量)+SiO2![]() 2MgO+Si,2Mg+Si
2MgO+Si,2Mg+Si![]() Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体;③Mg在加热时能与CO2、N2反应。
Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体;③Mg在加热时能与CO2、N2反应。
I.如图是实验室进行Mg与SiO2反应的裝置:

(1)盛放稀硫酸的装置为_________________,由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用_________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示为 ①____________________; ②_________________。
II.利用如图装置(量气管“0”刻度在刻度线的最上方)可测定生成物的纯度。

(3)实验开始前应先_________________。
(4)若取样品Wg加入5mLNaOH(足量)充分反应。反应前量气管液面读数为V1mL,反应后为V2mL(实验数据均转化为标准状况下),则样品的纯度为____________________。(写出计算式,不化简)。
(5)若反应结束时读数前未调节量气装置两边液面高度相平(右边的液面高于左边液面),则会导致实验结果______(填“偏高”、“偏低”或“无影响”)。
【答案】分液漏斗 b Mg2Si+4HCl=2MgCl2+SiH4↑ SiH4+2O2=SiO2+2H2O 检查装置气密性 ![]() 偏低
偏低
【解析】
(1)根据仪器构造分析其名称;Mg为活泼金属,在空气中点燃可以和O2、CO2、H2O反应,在工业中利用镁制取硅需排尽装置中的空气,据此判断X气体;
(2)根据题干中的已知信息分析判断;
(3)根据装置不能漏气解答;
(4)根据反应中产生的氢气与硅的物质的量之间的关系解答;
(5)根据压强对气体体积的影响分析解答。
(1)根据装置图可判断盛放稀硫酸的装置为分液漏斗;由于在点燃的条件下Mg可以与O2、CO2反应发生化学反应生成氧化镁、氧化镁和碳,Mg与氢气不能发生反应,因此可用氢气作为保护气,选用的药品为稀硫酸和锌粒,再用浓硫酸干燥,所以试管中的固体药品可选用锌粒,答案选b;
(2)Mg2Si遇盐酸迅速反应生成SiH4(硅烷),其反应的方程式为:Mg2Si+4HCl=2MgCl2+SiH4↑,SiH4常温下是一种不稳定、易自燃的气体,反应的方程式为SiH4+2O2=SiO2+2H2O,所以往反应后的混合物中加入稀盐酸,可观察到闪亮的火星;
(3)反应中有气体产生,所以实验开始前应先检查装置气密性;
(4)若取样品Wg加入5mLNaOH(足量)充分反应。反应前量气管液面读数为V1mL,反应后为V2mL(实验数据均转化为标准状况下),则反应中产生氢气的体积是(V1―V2―5)mL,物质的量是![]() ,根据1mol硅失去4mol电子可知消耗硅的物质的量是
,根据1mol硅失去4mol电子可知消耗硅的物质的量是![]() ,质量是
,质量是![]() ,因此样品的纯度为
,因此样品的纯度为![]() ;
;
(5)若反应结束时读数前未调节量气装置两边液面高度相平(右边的液面高于左边液面),说明装置内压强大于外界大气压,因此V1偏小,则会导致实验结果偏低。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】将物质X逐渐加入Y溶液中,生成沉淀物质的量n2与所加X的物质的量n1的关系如图所示。符合图所示情况的是
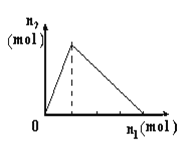
A | B | C | D | |
X | NaOH | AlCl3 | HCl | NaAlO2 |
Y | AlCl3 | NaOH | NaAlO2 | HCl |
A. A B. B C. C D. D
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=______,该条件下的平衡常数K=________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”“逆向”或“不”);最终达平衡时NO的转化率a=______________。
(3)在25 ℃下,向浓度均0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_____沉淀(填化学式),当两种沉淀共存时,溶液中c(Mg2+)/c(Cu2+)=__________(已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)。
【题目】回答下列有关问题。
(1)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
阳离子 | K+ | Cu2+ | Fe3+ | Al3+ | Fe2+ |
阴离子 | Cl- | CO32— | NO3— | SO42— | SiO32— |
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:原溶液中所含阳离子是___________________,阴离子是_____________________。
(2)光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

图1 图2
①图1中N型半导体为____________(填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___________________________________________。
③若A极产生7.00gN2,则此时B极产生_____________LH2(标准状况下)。