题目内容
3.用NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 46g乙醇中含有的化学键数为7NA | |
| B. | 1mol氯气和足量NaOH溶液反应转移电子数为2NA | |
| C. | 1mol OH- 和1 mol-OH(羟基)中含有的质子数均为9NA | |
| D. | 10L 0.1 mol•L-1 的Na2CO3溶液中,Na+、CO32- 总数为3NA |
分析 A.乙醇分子中含有5个碳氢键、1个碳碳键、1个碳氧键、1个氧氢键,总共含有8个共价键;
B.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂,1mol氯气转移了1mol电子;
C.羟基和氢氧根离子中都含有9个电子;
D.碳酸钠溶液中,碳酸根离子部分水解,导致碳酸根离子数目减少.
解答 解:A.46g乙醇的物质的量为1mol,每摩尔乙醇分子含有8mol共价键,所以46g乙醇中含有的化学键数为8NA,故A错误;
B.Cl2与NaOH溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,从方程式可知1mol氯气反应时转移1mol电子,即转移电子数为NA,故B错误;
C.1mol OH-和1mol-OH所含的质子数均为氧原子与氢原子的质子数之和,即含有的质子数均为9NA,故C正确;
D.10L 0.1mol•L-1的Na2CO3溶液中,因CO32-能水解,CO32-数目减少,故Na+、CO32-总数小于3NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的应用,考查学生的综合分析能力,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确羟基与氢氧根离子的组成与区别.

练习册系列答案
相关题目
13.为了鉴定溴乙烷中溴元素的存在,试分析下列各步实验,其中操作顺序合理的是( )
①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④用HNO3酸化溶液.
①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④用HNO3酸化溶液.
| A. | ①②③④ | B. | ②③④① | C. | ④③②① | D. | ②③①④ |
14.下列有关实验原理、方法和结论都正确的是( )
| A. | 实验室配置氯化铁溶液,将氯化铁固体溶于水,加盐酸抑制水解 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 | |
| D. | 已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
11.下列各组元素中,第一电离能依次减小的是( )
| A. | H Li Na K | B. | Na Mg Al Cl | C. | I Br Cl F | D. | F O N C |
18.设阿伏伽德罗常数为NA,下列说法正确的是( )
| A. | pH=1 的H2SO4溶液中所含H+的个数为0.1NA | |
| B. | 100mL 0.1mol•L-1的NH4Cl溶液所含NH4+的个数为0.01NA | |
| C. | 电解精炼铜的过程中,外电路转移NA个电子,阴极生成铜的质量为32g | |
| D. | 将2molSO2和10molO2充入一密闭容器中完全反应后,生成SO3的分子数为2NA |
8.下列离子方程式正确的是( )
| A. | NH4HCO3 溶液中加入等物质的量浓度等体积的澄清石灰水:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| B. | Ca(ClO)2 溶液中加入Na2SO3 溶液 Ca2++SO32-═CaSO3↓ | |
| C. | 食醋溶解蛋壳:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO- | |
| D. | 将少量CO2气体通入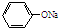 溶液中:CO2+H2O+ 溶液中:CO2+H2O+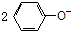 → →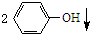 +CO32- +CO32- |
15.下列反应既利用了浓硫酸的强氧化性,又利用了浓硫酸的酸性的是( )
| A. | 碳与浓硫酸加热 | B. | 浓硫酸与NaCl固体加热 | ||
| C. | 浓硫酸中加入铜片 | D. | 蔗糖与浓硫酸混合后炭化发黑 |
12.G.X.Y.Z.Q均为氯(Cl)的含氧化合物,它们有如下关系:
①G→Q+NaCl
②Q+H2O-→X+H2
③Y+NaOH→G+Q+H2O
④Z+NaOH→Q+X+H2O
这五种化合物中,氯的化合价由低到高的顺序是( )
①G→Q+NaCl
②Q+H2O-→X+H2
③Y+NaOH→G+Q+H2O
④Z+NaOH→Q+X+H2O
这五种化合物中,氯的化合价由低到高的顺序是( )
| A. | QGZYX | B. | GYQZX | C. | GYZQX | D. | ZXGYQ |
13.下列说法中不正确的是( )
| A. | 元素电负性越大的原子,吸引电子的能力越强 | |
| B. | 在NH4+ 和[Cu(NH3)4]2+中都存在配位键 | |
| C. | 在晶体钋(简单立方堆积)中,每个钋原子周围紧密相邻的钋原子有8个 | |
| D. | CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为配位键 |