题目内容
【题目】(1)已知①H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
②CH4 (g)+![]() O2(g)=CO (g)+2H2O(g) ΔH=-564.3kJ·mol-1
O2(g)=CO (g)+2H2O(g) ΔH=-564.3kJ·mol-1
则CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:___。
(2)根据键能数据计算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热 ΔH=___kJ·mol-1。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(3)氢气是合成氨反应的重要原料。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟合成氨的工业化生产:N2(g)+3H2(g)![]() 2NH3(g) △H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示。
2NH3(g) △H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示。

回答下列问题:
①平衡时,M点NH3的体积分数为10%,则N2的物质的量为___(保留两位有效数字)。
②X轴上a点的数值比b点__(填“大”或“小”);图中,Y轴表示__(填“温度”或“压强”),判断的理由是__。
【答案】CH4(g)+H2O(g)=CO(g)+3H2(g),ΔH=+161.1kJ·mol-1 -1940 0.82mol 小 温度 随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)![]() 2NH3(g) △H<0向逆反应方向移动,故Y为温度
2NH3(g) △H<0向逆反应方向移动,故Y为温度
【解析】
(1)有盖斯定律知:②-①×3得:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=-564.3kJ·mol-1-3×(-241.8kJ·mol-1)=+161.1kJ·mol-1
(2)△H=反应物键能之和生成物键能之和,结合图表中 键能数据可知△H=414KJ/mol×4+4×155KJ/mol(489KJ/mol×4+4×565KJ/mol)=1940KJ/mol,
故答案为:1940 kJmol1;
(3)①设转化的氮气为xmol,则:N2(g)+3H2(g)2NH3(g)
起始量(mol):1 3 0
转化量(mol):x 3x 2x
平衡量(mol):1-x 3-3x 2x
所以(2x)2÷{(1-x)×(3-3x )3}==10%,解得x=0.18mol
mol,故氮气的物质的量是1mol-0.18mol=0.82mol;
故答案为:0.82mol;
②有图像可知X轴上a点的数值比b点小,随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)2NH3(g)△H<0向逆反应方向移动,正反应为体积减小的放热反应,故Y为温度,则X为压强,增大压强平衡正向移动;
故答案为:小;温度;随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)2NH3(g)△H<0向逆反应方向移动,故Y为温度;

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】一氯氨、二氯氨和三氯氨(NH2Cl、NHCl2和NCl3)是常用的饮用水二级消毒剂。
(1)用Cl2和NH3反应制备三氯胺的方程式为3Cl2(g)+NH3(g)NCl3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
t /min | 0 | 40 | 80 | 120 | 160 |
甲(400℃)n(Cl2)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙(T℃)n(Cl2)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①T℃_____400℃(填“>”或“<”),该反应的ΔH____0(填“>”或“<”)。
②该反应自发进行的条件是__________(填高温、低温、任何温度)。
③对该反应,下列说法正确的是_________(填选项字母)。
A. 若容器内气体密度不变,则表明反应达到平衡状态
B. 若容器内Cl2和NH3物质的量之比为3∶1,则表明反应达到平衡状态
C. 反应达平衡后,其他条件不变,加入一定量的NCl3,平衡将向逆反应方向移动
D. 反应达到平衡后,其他条件不变,在原容器中按![]() 继续充入一定量反应物,达新平衡后Cl2的转化率增大
继续充入一定量反应物,达新平衡后Cl2的转化率增大
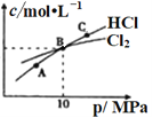
(2)工业上可利用反应2Cl2(g)+NH3(g)NHCl2(l)+2HCl(g)制备二氯胺。
①NHCl2在中性、酸性环境中会发生强烈水解,生成具有强杀菌作用的物质,写出该反应的化学方程式______________________________。
②在恒温条件下,将2molCl2和1molNH3充入某密闭容器中发生上述反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示。则A、B、C三点中Cl2转化率最高的是________点(填“A”“B”或“C”);B点时反应物转化率:α(Cl2)____α(NH3)(填“>”“=”或“<”),若B点平衡体积为2L,则平衡常数K=_____________。