题目内容
【题目】已知A(g)+B(g)=2C(g),反应过程中C的百分含量与温度关系如图,下列正确的是

A.正反应速率:v(c)>v(d)>v(b)
B.化学平衡常数:K(d)>k(c)
C.c向d变化时,v(正)<v(逆)
D.d点状态加入合适的催化剂可使c%增大
【答案】C
【解析】
由图可知,T1~T3为平衡的建立,c为平衡点,平衡后T3~T4段中C的含量减小,可知升高温度平衡逆向移动,正反应为放热反应,且K与温度有关,温度越高速率越大。
A、温度越高速率越大,则正反应速率v(d)>v(c)>v(b),故A错误;
B、正反应为放热反应,升高温度平衡逆向移动,K减小,则化学平衡常数:K(d)<K(c),故B错误;
C、由c向d变化时,平衡逆向移动,可知v(正)<v(逆),故C正确;
D、d点时加入催化剂不会使平衡移动, c%不变;故D错误。
答案选C。

【题目】(1)已知①H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
②CH4 (g)+![]() O2(g)=CO (g)+2H2O(g) ΔH=-564.3kJ·mol-1
O2(g)=CO (g)+2H2O(g) ΔH=-564.3kJ·mol-1
则CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:___。
(2)根据键能数据计算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热 ΔH=___kJ·mol-1。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(3)氢气是合成氨反应的重要原料。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟合成氨的工业化生产:N2(g)+3H2(g)![]() 2NH3(g) △H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示。
2NH3(g) △H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示。

回答下列问题:
①平衡时,M点NH3的体积分数为10%,则N2的物质的量为___(保留两位有效数字)。
②X轴上a点的数值比b点__(填“大”或“小”);图中,Y轴表示__(填“温度”或“压强”),判断的理由是__。
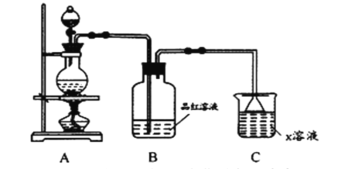
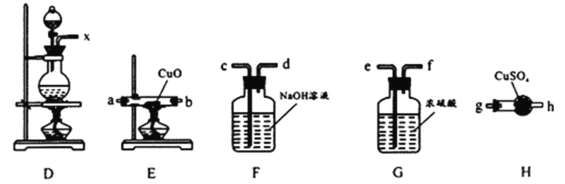
【题目】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分: 琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物(见图)。该药品不溶于水但能溶于人体中的胃酸(主要成分:稀盐酸),服用时同维生素 C一起服用效果会更好。某学习小组为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:


(1)试剂1是_____________。
(2)取少量B溶液于试管中,向其滴加NaOH溶液。最初观察到白色沉淀,一会灰变为灰绿色,最终变为红褐色,沉淀颜色变化的原因是_________________(用化学方程式表示)。
(3)B溶液中加入KSCN溶液后,溶液中也产生了红色,其可能的原因是____________。
(4)有同学提出由C到D 用双氧水代替新制氯水效果会更好原因是____,写出用双氧水实现由C到D转变的离子方程式________。
(5)在上述实验中,同学们发现血红色溶液放置一段时间后,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙两位同学首先对此进行了猜想:
编号 | 猜想 |
甲 | 溶液中的+3价Fe又被还原成+2价铁 |
乙 | 溶液中的SCN-被过量的新制氯水氧化 |
①你认为甲同学的猜想合理吗______?(填“合理”或“不合理”)请说明理由_______。
②基于乙同学的猜想,请设计一个简单的实验加以验证____________________________。
(6)“速力菲”药品为什么要与维生素 C一起用效果会更好原因是_______。
【题目】以镍废料(主要成分为镍铁合金,含少量铜)为原料,生产NiO的部分工艺流程如下:
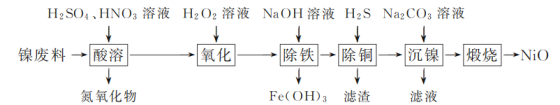
已知:下表列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.3 | 9.9 | 9.2 |
(1) “酸溶”时Ni转化为NiSO4,该过程中温度控制在70~80 ℃的原因是________。
(2) “氧化”时,Fe2+参加反应的离子方程式为________。
(3) “除铁”时需控制溶液的pH范围为________。
(4) “滤渣”的主要成分为________(填化学式)。
(5) “沉镍”时得到碱式碳酸镍[用xNiCO3·yNi(OH)2表示]沉淀。
①在隔绝空气条件下,“煅烧”碱式碳酸镍得到NiO,该反应的化学方程式为________。
②“沉镍”时,溶液pH增大,碱式碳酸镍中Ni元素含量会增加,原因是________。