题目内容
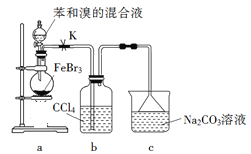
【题目】石灰石一石膏法脱硫是除去工业烟气中所含SO2的重要方法,其工艺分为两步:一是吸收SO2产生亚硫酸氢钙,二是氧化产生石膏。某校化学兴趣小组实验模拟该工艺,设计置如下:

(1)装置B模拟产生含SO2的工业烟气,则E装置的作用是_______________。
(2)实验开始时,打开装置B中分液漏斗的活塞,向烧瓶中逐滴滴加硫酸,D中立即产生了明显的现象造成产生这一现象的原因是________。
A.该装置的气密性不够好
B.滴加硫酸的速率较快
C.使用的硫酸浓度较小
D.石灰石浆液中碳酸钙粉末的颗粒太小
(3)预计当装置C中________________的现象时,关闭装置B中分液漏斗的活塞,再点燃装置A处的酒精灯。实际实验过程中却始终未观察到C中产生这一现象,小组成员多次进行实验探究,最终发现是药品Na2SO3部分变质,请写出定性实验发现药品Na2SO3问题的有关操作及现象:取少量的亚硫酸钠固体于试管中,______________________。
【答案】除去尾气中的SO2 B 由浑浊变澄清 先加适量的水溶解,再加入足量的盐酸与氯化钡溶液,有白色沉淀生成
【解析】
(1)二氧化硫气体有毒,所以E装置中的碱液是除去尾气;
(2)D中因为产生气流速率太快,所以出现明显现象,由此分析产生速率过快的原困;
(3)二氧化硫与碳酸钙反应生成可溶于水的亚硫酸氢钙和二氧化碳气体;检验亚硫酸钠是否变质,可取少量的亚硫酸钠固体于试管中,先加适量的水溶解,再加入足量的盐酸与氯化钡溶液,有白色沉淀生成。
(1)二氧化硫气体有毒,不能直接排放到空气中,所以E装置中的碱液是除去尾气中的SO2,防止污染大气;
(2)A.该装置的气密性不够好,气流速率减慢,二氧化硫的量减少,所以不会出现明显的现象,A错误;
B.滴加硫酸的速率较快,气流速率加快,所以出现明显的现象,B正确;
C.使用的硫酸浓度较小,产生气流速率减慢,C错误;
D.石灰石浆液中碳酸钙粉末的颗粒太小,导致二氧化硫消耗速率加快,所以产生气流速率减慢,D错误;
故合理选项是B;
(3)二氧化硫与碳酸钙反应生成可溶于水的亚硫酸氢钙和二氧化碳气体,所以装置C中产生的现象为由浑浊变澄清;检验亚硫酸钠是否变质的操作是:取少量的亚硫酸钠固体于试管中,先加适量的水溶解,再加入足量的盐酸与氯化钡溶液,有白色沉淀生成。

【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D