题目内容
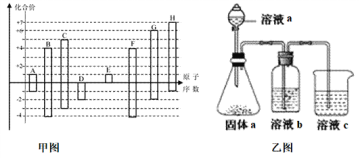
【题目】已知SO2通入BaCl2溶液无明显现象。某同学利用如图装置探究SO2与BaCl2溶液反应生成白色沉淀的条件。下列判断正确的是
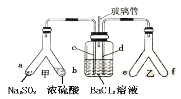
A.e、f两管中的试剂可以分别是浓氨水和NaOH固体
B.乙中产生的一定为氧化性气体,将BaSO3氧化为BaSO4沉淀
C.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
D.c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
【答案】A
【解析】
SO2与BaCl2反应产生沉淀,溶液中必须存在大量的SO32-,右侧Y型管中应能生成碱性气体或氧化性气体,若是碱性气体,溶液中存在大量的SO32-,若是氧化性气体,溶液中可生成SO42-,则生成的沉淀可能为BaSO3或BaSO4;容器内压强增大,溶液倒吸,气体不容易导入,所以导气管A的作用是保持集气瓶内外气压平衡,以便左右两边产生的气体顺利导入,由此分析解答。
A. 若是碱性气体,溶液中存在大量的SO32,所以e、f两管中的试剂可以分别是浓氨水和NaOH,产生氨气碱性气体,故A正确;
B. SO2与BaCl2不反应,氧化性气体将溶液中的亚硫酸根离子氧化成硫酸根离子,而不是将BaSO3氧化为BaSO4沉淀,故B错误;
C. 玻璃管的作用是连通大气,平衡压力,以便左右两边产生的气体顺利导入,故C错误;
D. 如果产生氨气,氨气极易溶于水,为防止倒吸,所以不能插入BaCl2溶液中,故D错误;
答案选A。

练习册系列答案
相关题目