题目内容
5.工业上用铝土矿(主要成分为Al2O3•H2O,Al2O3•3H20以及少量Fe2O3、SiO2)提取纯Al2O3做冶炼铝的原料,提取的操作过程用下面的流程图表示:
(1)滤液A中溶质的化学式为:AlCl3,FeCl3,HCl,
(2)写出滤液A中的一种溶质与过量NaOH反应形成滤液B中溶质的离子方程式:Al3++4OH-=AlO2-+2H2O.
(3)如将第③步通CO2改为加过量盐酸,最后能否得到Al2O3不能.
分析 由流程可知,加盐酸,只有SiO2不反应,氧化铝、氧化铁均与盐酸反应,过滤沉淀为SiO2;滤液A中加过量NaOH,铝离子转化为偏铝酸钠,铁离子转化沉淀,过滤后,滤液B与二氧化碳反应生成氢氧化铝和碳酸氢钠,最后氢氧化铝分解生成氧化铝,以此来解答.
解答 解:(1)①氧化铝与盐酸反应生成氯化铝和水,反应方程式为Al2O3+6HCl═2AlCl3+3H2O,氧化铁与盐酸反应生成氯化铁与水方程式为Fe2O3+6HCl═2Fe2Cl3+3H2O,所以滤液A中含有氯化铝、氯化铁、氯化氢,
故答案为:AlCl3,FeCl3,HCl;
(2)氯化铝与氢氧化钠反应生成四羟基合铝酸钠与氯化钠,反应的离子方程式为Al3++4OH-=AlO2-+2H2O,
故答案为:Al3++4OH-=AlO2-+2H2O;
氯化铁与氢氧化钠反故答案为应生成氢氧化铁和氯化钠,反应方程式为 FeCl3+3NaOH═Fe(OH)3↓+3NaCl;
(3)如将第③步通CO2改为加过量盐酸,偏铝酸钠溶液和过量盐酸反应生成氯化铝溶液,得不到氢氧化铝沉淀,最后不能得到Al2O3,
故答案为:不能.
点评 本题考查混合物分离提纯方法的综合应用,为高频考点,把握流程中的反应及化学反应方程式书写为解答的关键,侧重分析、实验能力及化学用语的考查,题目难度不大.

练习册系列答案
相关题目
13.在水中加入下列物质,能促进水的电离且溶液为碱性的是( )
| A. | H2SO4 | B. | NH4Cl | C. | CH3COONa | D. | NaOH |
20.将物质的量相同的NH3•H2O和NH4Cl混合配成溶液,则下列关系错误的是( )
| A. | c(OH-)>c(H+) | B. | c(NH4+)>c(NH3•H2O) | ||
| C. | c(NH4+)>c(H+)=c(OH-)>c(Cl-) | D. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
10.下列物质加入水中,能使水的电离度增大且溶液显酸性的是( )
| A. | Al2(SO4)3 | B. | HCl | C. | Na2S | D. | NH3.H2O |
17.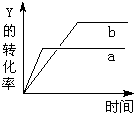 反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
 反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )| A. | 加入催化剂 | B. | 增大压强 | C. | 降低温度 | D. | 增大Y的浓度 |
14.X、Y、Z均为短周期元素,其简单离子X+、Y3+、Z2-的核外电子层结构相同.下列说法不正确的是( )
| A. | 离子半径:X+>Y3+>Z2- | B. | 碱性:XOH>Y(OH)3 | ||
| C. | 单质的还原性:X>Y | D. | 原子序数:Y>X>Z |
13.下列有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H20 | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)