题目内容
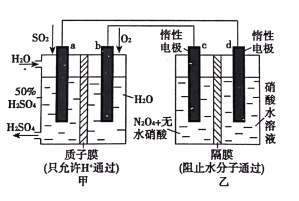
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是
A. 电极b反应式是O2+4e-+2H2O=4OH-
B. 乙装置d电极附近溶液的pH增大
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 每转移2mole-生成2molN2O5和1molH2SO4
【答案】D
【解析】
A.甲装置为原电池,其中a电极为负极、b电极为正极,左侧加入了硫酸,其中的H+可透过质子膜而进入右侧极室,所以右侧极室是酸性的,所以电极反应中不能生成OH-,而应生成水:O2+4e-+4H+=2H2O,A项错误;
B.乙装置是一个电解池,均采用了惰性电极,左侧为阳极,右侧d电极为阴极,其中盛放了硝酸溶液,发生的反应为:2H++2e-=H2↑,虽然消耗了H+,但同时有等量的H+从阳极区迁移过来,故溶液的pH不变,B项错误;
C.c电极为阳极,发生氧化反应:N2O4-2e-+2HNO3=2N2O5+2H+,C项错误;
D.据C项的电极反应式N2O4-2e-+2HNO3=2N2O5+2H+,可以看出转移2mole-生成2molN2O5,根据甲装置的左侧的电极反应式:SO2-2e-+2H2O=4H++SO42-,可知转移2mole-生成1molH2SO4,D项正确;
答案选择D项。

练习册系列答案
相关题目