题目内容
【题目】下列有关溶液中微粒的物质的量浓度关系正确的是( )
A. 某弱酸的酸式盐NaHA溶液中一定有:c(OH﹣)+2c(A2﹣)=c(H+)+c(H2A)
B. 0.2 molL﹣1 CH3COONa溶液与0.1 molL﹣1盐酸等体积混合后的酸性溶液中:c(CH3COO﹣)>c(CH3COOH)>c(Cl﹣)>c(H+)
C. 室温下,向100ml0.5mol/L的Na2CO3溶液中加入0.05molCaO,  溶液中增大
溶液中增大
D. 0.1 molL﹣1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3H2O)+c(Fe2+)=0.3 molL﹣1
【答案】C
【解析】A. 任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH)+c(HA)+2c(A2),根据物料守恒得c(HA)+c(A2)+c(H2A)=c(Na+),联立两式得c(OH)+c(A2)=c(H2A)+c(H+),故A错误;B. 0.2 molL﹣1 CH3COONa溶液与0.1 molL﹣1盐酸等体积混合,得到等浓度的醋酸钠、氯化钠和醋酸的混合溶液,溶液显酸性,说明醋酸的电离程度大于醋酸根离子的水解程度, 则c(CH3COOH)<c(Cl),故B错误;C. 氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,溶液中氢氧根浓度增大,消耗碳酸根离子,则溶液中碳酸氢根离子浓度减小,溶液中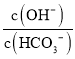 增大,故C正确;D. 0.1 molL﹣1 (NH4)2Fe(SO4)2溶液中存在物料守恒:c(NH4+)+c(NH3H2O)+c(Fe2+)+c[Fe(OH)2]=0.3 molL1,故D错误;答案选C。
增大,故C正确;D. 0.1 molL﹣1 (NH4)2Fe(SO4)2溶液中存在物料守恒:c(NH4+)+c(NH3H2O)+c(Fe2+)+c[Fe(OH)2]=0.3 molL1,故D错误;答案选C。

练习册系列答案
相关题目